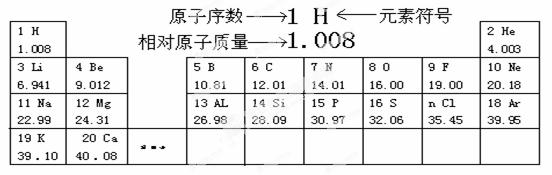
��Ŀ����
����̽��С���ʵ���ʦ�ṩ��һ����ɫ���壨������NaCl��Na2SO4��Na2CO3��NaNO3��һ�ֻ��֣������������ʵ�飬��ÿ��ʵ���о������������Լ�������ַ�Ӧ��ʵ����̡������ͼ��

�����ʵ����̲�����������⣺
��1��ʵ���в�����ϡ�������ϡ�����ԭ����������
��2������ϡHNO3ʱ������Ӧ�Ļ�ѧ����ʽΪ�������μ�Ba��NO3��2��Ŀ����������
��3��ͨ������������ƶ�ԭ��ɫ����ijɷֿ�����������
| ���ʵļ����ƶϣ���Ļ�ѧ���ʣ��εĻ�ѧ���ʣ���д��ѧ����ʽ�����ֱ���ʽ�����뷽��ʽ��. | |
| ר�⣺ | �������ɵ��ƶ��⣮ |
| ������ | ��1�����������е�������Ҳ������������Ӧ���ɰ�ɫ����������Ȼ��Ƶļ�����ɸ��Ž��з����� ��2���������е������ζ�����ˮ�������̼���η�Ӧ���ɶ�����̼���壬�����ӻ�����������ӷ�Ӧ���ɰ�ɫ�����ᱵ�������з����� ��3�������������̼���Ʒ�Ӧ���ɶ�����̼���壬���ᱵ���������Ʒ�Ӧ�������ᱵ�������з����� |
| ��� | �⣺��1��ͨ��ת��ͼ�����ӵ��Լ����Կ�����������������Ϊ�˼����Ȼ��ƵĴ��ڣ�������������ᣬ�����������ӣ����Ȼ��Ƶļ�����ɸ��ţ�����ʵ���в�����ϡ�������ϡ�����ԭ���ǣ���ֹϡ������AgNO3��Һ��Ӧ�����ж��Ƿ���NaCl��ɸ��ţ� ��2��������������ɫ���������˵����ɫ�����к�̼���ƣ�̼���ƺ���������������ơ�ˮ�Ͷ�����̼�����е������ζ�����ˮ�������ӻ�������������������ᱵ��ɫ���������Եμ�Ba��NO3��2��Ŀ���ǣ������ɫ�������Ƿ���Na2SO4�� ��3��������������ɫ���������˵����ɫ������һ����̼���ƣ��������ᱵ����������˵����ɫ�����в��������ƣ����е��������ж��Ƿ��������ƣ��Ȼ��ƺ��������������Ȼ��������������ƣ�����ԭ��ɫ������һ�������Ȼ��ơ�̼���ƣ����ܺ��������ƣ� �ʴ�Ϊ����1��������������Ӹ��ź���ļ��飻 ��2��Na2CO3+2HNO3�T2NaNO3+H2O+CO2���������Ƿ��������ƣ� ��3��NaCl��Na2CO3�� |
| ������ | �ڽ������ʱ�����ȷ�������������и����ʵ����ʣ�Ȼ���������������ʵ����������жϣ����ȷ����������ɳɷ֣� |

 53���ò�ϵ�д�
53���ò�ϵ�д�2012��6��18�����۾źŷɴ����칬һ��Ŀ�������ʵ���Զ�����Խӣ������й�ʵʩ���״����˿ռ佻��Խӣ��칬һ��Ŀ��������������ص��ܷ�ӦʽH2+2NiO��OH��=2Ni��OH��2��������������ȷ���ǣ�������
| �� | A�� | H2�ǵ��� |
| �� | B�� | NiO��OH��2�������� |
| �� | C�� | �μӷ�Ӧ��H2��NiO��OH����������Ϊ1��92 |
| �� | D�� | ����Ӱ����ʱ���ɵ�������ɴ����й��磬����ѧ��ת��Ϊ���� |
���������ж�����ˮ������������Ũ�������������������Ƹ�����ǣ�������
| �� | A�� | SO2 | B�� | HCl | C�� | O2 | D�� | CO2 |
ijͬѧΪ�˲ⶨ��ͭм����п��ͭ�γɵĺϽ���Ʒ��ɣ�ȡ�ķ���Ʒ�ֱ��ϡ���ᷴӦ�����õ���ʵ�����ݻ��Ƴ���ͼ����ʵ�����ݼ�¼���±���
| ��Ʒ | ��1�� | ��2�� | ��3�� | ��4�� |
| ȡ��Ʒ������g�� | 50.0 | 50.0 | 50.0 | 50.0 |
| ȡϡ����������g�� | 40.0 | 80.0 | 120.0 | 160.0 |
| ��������������g�� | 0.4 | 0.8 | 1.0 | 1.0 |
�Իش�
��1�����������ڵ�1����Ʒ��õ������У������������ʣ���ȫ��Ӧ�ˣ�
��2����ʽ�����ͭм��Ʒ�е�п������������
��3������ϡ���������ʵ�����������

��������������������ǣ�������
| �� | A�� | ��ʯ�ң�CaO�� | B�� | Һ̬����O2 �� | C�� | �Ȼ��ƣ�CaCl2�� | D�� | �ռNaOH�� |
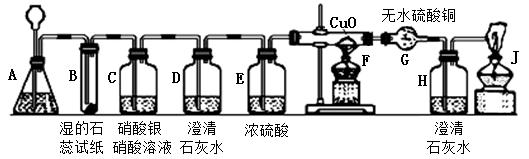
 D.������һ��ֻ��һ��Ԫ��
D.������һ��ֻ��һ��Ԫ�� ��һ���֣�Ԫ��������ʡ�ԣ���
��һ���֣�Ԫ��������ʡ�ԣ���