题目内容
7.根据下列装置,结合所学化学知识回答下列问题.
(1)写出仪器①的名称集气瓶.
(2)实验室选择装置B用高锰酸钾制取氧气时,在试管口放一团棉花的目的是防止高锰酸钾进入导气管,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室可以选择装置AD(填字母)组合来制取并收集CO2气体,检验CO2是否收集满的方法是将燃着的木条放于集气瓶口,若木条熄灭则收集满了.
(4)通常情况下,SO2是一种无色、有刺激性气味的气体,密度比空气大,易溶于水且水溶液显酸性.实验室里,常用盐硫酸钠固体和浓硫酸反应制取SO2.实验室制取SO2选择的发射装置是A(填字母),若选择F装置收集SO2,气体应该从a(填“a”或“b”)进入.实验结束后,剩余的SO2气体可用氢氧化钠溶液吸收,吸收的目的是防止造成空气污染.
分析 (1)熟记常见仪器的名称;
(2)根据实验室中用高锰酸钾制取气体的注意事项来解答,并完成化学方程式的书写;
(3)实验室制取二氧化碳用大理石和稀盐酸,属于固液常温型,二氧化碳的密度比空气大且能溶于水,据此选择发生和收集装置,利用燃着的木条放于集气瓶口观察是否熄灭进行验满;
(4)根据用亚硫酸钠固体和浓硫酸反应制取SO2属于固体和液体混合不需要加热的反应以及二氧化硫的密度大于空气的密度进行解答.
解答 解:(1)仪器①的名称是集气瓶;故填:集气瓶;
(2)高锰酸钾在加热的条件下可以分解产生二氧化锰、锰酸钾和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;高锰酸钾呈粉末状,在加热时容易进入导管而堵塞导管,所以要在试管口放一团棉花;故填:防止高锰酸钾进入导气管;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取二氧化碳用大理石和稀盐酸,属于固液常温型,故选发生装置A,二氧化碳的密度比空气大且能溶于水,故用向上排空气法收集;利用燃着的木条放于集气瓶口观察是否熄灭进行验满;故填:AD;将燃着的木条放于集气瓶口,若木条熄灭则收集满了;
(4)用亚硫酸钠固体和浓硫酸反应制取SO2属于固体和液体混合不需要加热的反应,所以实验室制取SO2选择的发生装置是B;二氧化硫的密度大于空气的密度,所以若选择F装置收集SO2气体,气体应该从d端进入.二氧化硫是一种有毒的气体,为了防止造成空气污染,所以用氢氧化钠溶液进行吸收;故答案为:A;a;防止造成空气污染.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案| A. | H2SO4 | B. | HCl | C. | Cu(OH)2 | D. | Ca(OH)2 |
| A. |  粮食酿酒 | B. |  棉纱织布 | C. |  火药应用 | D. |  瓷器烧制 |
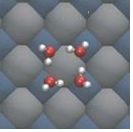 近年,我国科学家首次拍摄到水分子团簇图象,模型如图.下列说法正确的是( )
近年,我国科学家首次拍摄到水分子团簇图象,模型如图.下列说法正确的是( )| A. | 氢氧两种元素只能组成水 | B. | 团簇中的水分子不再运动 | ||
| C. | 水蒸气冷凝成水,分子间隔减小 | D. | 可燃冰和冰都是由水分子构成 |
| A. | 两个氧分子:2O | B. | 三个二氧化硫分子:3SO2 | ||
| C. | 水中氧元素的化合价为-2价:H2$\stackrel{2-}{O}$ | D. | 一个钙离子:Ca+2 |
| A. | 为了加快固体溶解,可用温度计搅拌 | |
| B. | 直接点燃未经验纯的可燃性气体 | |
| C. | 稀释浓硫酸时,将浓硫酸沿烧杯壁缓慢地注入水里,并不断搅拌 | |
| D. | 加热后的试管立即用冷水冲洗 |
 C60发现使人类了解到一个全新的碳世界,根据图1回答下列问题:
C60发现使人类了解到一个全新的碳世界,根据图1回答下列问题: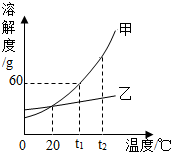 水是生命之源,人类的生产、生活离不开水.
水是生命之源,人类的生产、生活离不开水.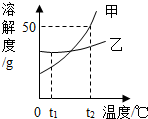 如图是甲、乙两种固体物质的溶解度曲线.请回答:
如图是甲、乙两种固体物质的溶解度曲线.请回答: