题目内容
13.t℃时将15g碳酸钙粉末与一定的盐酸恰好完全反应,反应后得饱和溶液,其溶质的质量分数为25%,求:(1)反应可制得二氧化碳多少克?
(2)所用盐酸中溶质的质量分数是多少?(精确计算0.1%)
分析 (1)根据碳酸钙的质量可计算二氧化碳的质量;
(2)欲求盐酸中溶质的质量分数,先求出盐酸溶质质量和溶液质量;
根据15g碳酸钙粉末与一定质量的盐酸恰好完全反应,可求出溶质盐酸的质量;
根据反应后所得氯化钙溶液饱和溶液的溶质的质量分数为25%和生成氯化钙的质量,求出饱和溶液的质量;
根据质量守恒定律,反应前后物质的质量相等的关系求得盐酸的质量;
根据溶质质量分数质量分数公式即可解答.
解答 解:设15gCaCO3消耗HCl的质量为x,生成CaCl2的质量为y,生成CO2的质量为z
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 111 44
15g x y z
$\frac{100}{15g}=\frac{73}{x}=\frac{111}{y}=\frac{44}{z}$
x=10.95g;y=16.65g;z=6.6g
反应后所得CaCl2饱和溶液的质量为:16.65g÷25%=66.6g
盐酸的质量为:66.6g+6.6g-15g=58.2g
盐酸中溶质的质量分数为:$\frac{10.95g}{58.2g}$×100%=18.8%.
答:(1)反应可制得二氧化碳6.6克;
(2)所用盐酸中溶质的质量分数是18.8%.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
1.要除去一氧化碳气体中混有的少量二氧化碳气体,应采用的方法是( )
| A. | 将混合气体通过足量的石灰水 | |
| B. | 将混合气体从一个容器倒入另一个容器 | |
| C. | 将混合气体通过灼热的氧化铜粉末 | |
| D. | 将混合气体通入水中 |
8.把铁片分别放入下列物质的溶液中,过一段时间取出,溶液质量增加的是( )
| A. | ZnSO4 | B. | CuSO4 | C. | H2SO4 | D. | AgNO3 |
18.A、B、C三只小烧杯内分别依次盛有一定体积的浓氨水、酚酞溶液、酚酞溶液,按如图所示进行探究活动,不能得到的结论是( )
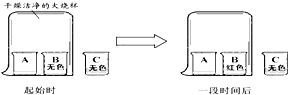

| A. | 氨水能使酚酞溶液变红 | B. | 分子间有间隙 | ||
| C. | 分子在不断地运动 | D. | 浓氨水易挥发,氨气易溶于水 |
5.把100克10%的硝酸钾溶液的浓度提高一倍,正确的方法是( )
| A. | 再溶解10克硝酸钾 | B. | 蒸发掉50克水 | ||
| C. | 将溶液倒掉50克 | D. | 升高温度 |