题目内容
某地下水含有大量可溶于水的Ca(HCO3)2和Mg(HCO3)2..用试管取少量,加入肥皂水,振荡,出现大量浮渣和浑浊.,该水长期煮沸,锅底会产生一层白色固体(水垢).某化学小组对该白色固体的成分进行探究:
【提出猜想】猜想①白色固体是CaCO3猜想②白色固体是Mg(OH)2猜想③白色固体是CaCO3和Mg(OH)2
【设计实验】
【反思一评价】小组有同学认为的结论不够严密,理由是 .
【继续探究】同学们经过反复讨论提出了验证猜想③的实验方案:(以下微溶物视为易溶物)
上述步骤(1)中有关化学方程式是 (写一个)
【提出猜想】猜想①白色固体是CaCO3猜想②白色固体是Mg(OH)2猜想③白色固体是CaCO3和Mg(OH)2
【设计实验】
| 实验步骤(1) | 可能现象 | 结论 |
| 白色固体完全溶解, 有气泡产生 |
猜想①正确 |
【继续探究】同学们经过反复讨论提出了验证猜想③的实验方案:(以下微溶物视为易溶物)
| 实验步骤(2) | 可能现象 | 结论 |
| (1)取少量白色固体于试管中,向其中加入足量稀盐酸 | 白色固体完全溶解, 有气泡产生 |
猜想③成立 |
| (2)再向上述反应后的溶液中滴加足量 |
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【设计实验】运用碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳;
【反思一评价】根据碳酸钙和氢氧化镁混合也会出现相同的现象进行解答;
【继续探究】运用碳酸钙和氢氧化镁分别和盐酸反应的现象和氢氧化钠和氯化镁反应生成氢氧化镁白色沉淀和氯化钠解答.
【反思一评价】根据碳酸钙和氢氧化镁混合也会出现相同的现象进行解答;
【继续探究】运用碳酸钙和氢氧化镁分别和盐酸反应的现象和氢氧化钠和氯化镁反应生成氢氧化镁白色沉淀和氯化钠解答.
解答:解:【设计实验】根据现象结合碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,有气泡生成;氢氧化镁和稀盐酸反应生成氯化镁和水,固体溶解且无气泡生成,故实验步骤:
故填:取少量白色固体,加入足量稀盐酸;
【反思一评价】:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,有气泡生成;氢氧化镁和稀盐酸反应生成氯化镁和水,固体溶解且无气泡生成.含有碳酸钙出现此现象,若是碳酸钙和氯化镁的混合物也会出现此现象.故答案为:猜想③也有同样的现象;
【继续探究】为了验证白色固体中含有碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,白色固体溶解且有气泡生成;为了验证白色固体中含有氢氧化镁,氢氧化和稀盐酸反应生成氯化镁和水,氯化镁和氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠,故实验步骤:
上述步骤(1)中有关化学方程式是:2HCl+CaCO3=CaCl2+CO2↑+H2O、2HCl+Mg(OH)2=MgCl2+2H2O.
故答案为:NaOH溶液;有白色沉淀;CaCO3+2HCl=CaCl2+H2O+CO2(或 Mg(OH)2+2HCl=MgCl2+2H2O ).
| 实验步骤(1) | 可能现象 | 结论 |
| 取少量白色固体,加入足量稀盐酸 | 白色固体完全溶解, 有气泡产生 |
猜想①正确 |
【反思一评价】:碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,有气泡生成;氢氧化镁和稀盐酸反应生成氯化镁和水,固体溶解且无气泡生成.含有碳酸钙出现此现象,若是碳酸钙和氯化镁的混合物也会出现此现象.故答案为:猜想③也有同样的现象;
【继续探究】为了验证白色固体中含有碳酸钙,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,白色固体溶解且有气泡生成;为了验证白色固体中含有氢氧化镁,氢氧化和稀盐酸反应生成氯化镁和水,氯化镁和氢氧化钠反应生成氢氧化镁白色沉淀和氯化钠,故实验步骤:
| 实验步骤(2) | 可能现象 | 结论 |
| (1)取少量白色固体于试管中,向其中加入足量稀盐酸 | 白色固体完全溶解, 有气泡产生 |
猜想③成立 |
| (2)再向上述反应后的溶液中滴加足量NaOH溶液 | 有白色沉淀 |
| 实验步骤(2) | 可能现象 | 结论 |
| (1)取少量白色固体于试管中,向其中加入足量稀盐酸 | 白色固体完全溶解,有气泡产生 | 猜想③成立 |
| (2)再向上述反应后的溶液中滴加足量NaOH溶液 | 有白色沉淀物生成 | 猜想③成立 |
故答案为:NaOH溶液;有白色沉淀;CaCO3+2HCl=CaCl2+H2O+CO2(或 Mg(OH)2+2HCl=MgCl2+2H2O ).
点评:本题重点考查了碳酸钙和氢氧化镁与稀盐酸反应时现象的不同,侧重酸碱盐之间化学反应的考查,熟练掌握氢氧化镁和碳酸钙能和稀盐酸反应的性质和现象不难解答.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目

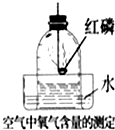 用红磷在钟罩中燃烧来测定空气中氧气的含量,发生的实验现象是:
用红磷在钟罩中燃烧来测定空气中氧气的含量,发生的实验现象是: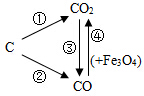 高炉炼铁过程中不是直接通入一氧化碳去与铁矿石反应,而是投入铁矿石和焦炭,鼓入高温空气.若高炉内投入的矿石是磁铁矿(Fe3O4),请写出各步变化的化学方程式:
高炉炼铁过程中不是直接通入一氧化碳去与铁矿石反应,而是投入铁矿石和焦炭,鼓入高温空气.若高炉内投入的矿石是磁铁矿(Fe3O4),请写出各步变化的化学方程式: