题目内容
4.A、B、C三个烧杯中盛有相同质量的水(期中A、C烧杯中水温为10℃,B烧杯中水温为30℃,不考虑溶解过程中水温的变化),分别加入甲、乙两种物质各10g,充分溶解后所得现象如图1所示,试回答: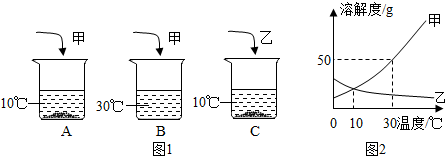
(1)你认为B烧杯的溶液可能是不饱和溶液;
(2)如图2是甲、乙两种物质的溶解度曲线图,按图分析,10℃时A、C烧杯中未溶解的溶质质量关系是相等(填“相等”或“不相等”).其它条件不变,将C烧杯中的温度升到50℃时,C烧杯中的溶液是饱和(填“饱和”或“不饱和”)溶液.
(3)若将A烧杯中溶质全部溶解,可采用的方法有:①升温,②加水(升温/加水).
(4)30℃时,100g水中溶解50g甲物质恰好达到饱和,该饱和溶液中溶质的质量分数为33.3%,若要把该饱和溶液稀释成质量分数为10%的溶液,应加水350g.
分析 (1)根据图1的可得到答案;
(2)根据溶解度曲线知10℃时甲、乙的溶解度相同解答;
(3)根据甲的溶解度曲线知,甲的溶解度随温度的升高而增大;
(4)根据溶液稀释前后溶质质量不变进行分析.
解答 解:(1)通过图1的可知,A、C两个烧杯充分溶解后,溶质部分未溶解,B中全部溶解,所以B烧杯中的溶液可能是不饱和溶液;
(2)有已知条件A、B、C 三个烧杯中盛有相同质量的水,10℃时甲、乙的溶解度相同,故分别加入甲、乙两物质各10g,充分溶解后A、C烧杯中未溶解的溶质质量关系是相等;由于乙的溶解度随温度的升高而减小,故其它条件不变,将C烧杯中的温度升到50℃时,C中会有新的晶体析出,故C烧杯中的溶液是饱和溶液;
(3)据甲的溶解度曲线知,甲的溶解度随温度的升高而增大,所以若将A烧杯中的溶质全部溶解,可采用的方法有升高温度和增加溶剂水;
(4)通过溶解度曲线可以看出,30℃时,100g水中溶解50g甲物质恰好达到饱和,该饱和溶液中溶质的质量分数为:$\frac{50g}{100g+50g}$×100%=33.3%,
设需要加水为x,
$\frac{50g}{100g+50g+x}$×100%=10%
x=350g
故答案为:(1)B;
(2)相等,饱和;
(3)①升温,②加水;
(4)50,33.3%,350.
点评 本题难度较大,主要考查了根据固体的溶解度曲线来解决相关的问题,从而培养学生的理解能力、分析能力和解决问题的能力.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
14.(1)用玻璃片盖上空集气瓶即可得空气;分别向两个盛满水倒立在水槽中的集气瓶缓缓吹气,直到把水全部排出,盖好玻璃片从水中取出集气瓶正放在桌上,就得到两瓶呼出的气体.
(2)填写下列空白:
(2)填写下列空白:
| 比较项目 | 实验操作 | 实验现象 | 得到结论 |
| 含氧气多少 | 将点燃的木条伸入空气中; 将点燃的木条伸入呼出的气体. | 空气中含有的氧气比呼出的气体中的多 | |
| 含二氧化碳多少 | 向一瓶空气和一瓶呼出的气体中各加入少量澄清的石灰水. | 只有向呼出的气体倒入澄清的石灰水变浑浊 | |
| 含水蒸气多少 | 呼气的玻璃片上有水雾 | 呼出的气体含水蒸气比空气中的多 |
15.保护地球是每个公民应尽的义务,下列做法对人类的生存环境会造成危害的是( )
| A. | 回收处理废旧电池 | B. | 使用无磷洗衣粉 | ||
| C. | 冰箱、空调使用含氯氟烃的制冷剂 | D. | 工业废水经处理达标后再排放 |
12.正确的实验操作是科学探究成功的基础,下列各项操作中错误的是( )
| A. |  闻气味 | B. | 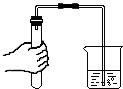 检查气密性 | ||
| C. | 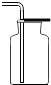 收集二氧化碳气体 | D. | 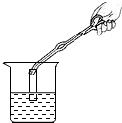 测定溶液的PH值 |
19.氢氧化钠的俗名不止一个.下列俗名不是表示氢氧化钠的是( )
| A. | 苛性钠 | B. | 纯碱 | C. | 烧碱 | D. | 火碱 |
9.以自行车代替汽车出行,可以减少我们现代生活中留下的“碳足迹”,积极应对全球气候变暖的严峻挑战.我们的各种行为留下的“碳足迹”可以用直观的“碳足迹计数器”进行估算.比如:
开车的二氧化碳排放量(kg)=汽油消耗升数×2.2
设骑车代替开车出行100Km,可以节约9L,则可以减排的二氧化碳约为( )
开车的二氧化碳排放量(kg)=汽油消耗升数×2.2
设骑车代替开车出行100Km,可以节约9L,则可以减排的二氧化碳约为( )
| A. | 100Kg | B. | 20Kg | C. | 9 Kg | D. | 2.2 Kg |
16.按下列装置实验,不能达到对应目的是( )
| A. | 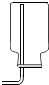 收集H2 | B. | 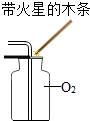 O2验满 | ||
| C. | 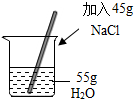 配制45%的NaCl溶液 | D. | 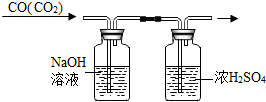 除去CO中的CO2 |