题目内容
12.含锌废渣和各种锌矿(如菱锌矿)都有着重要的用途,以含锌废渣(主要成分为ZnO,杂质为FeO﹑CuO)为原料制备七水硫酸锌(ZnSO4•7H2O)的流程如下: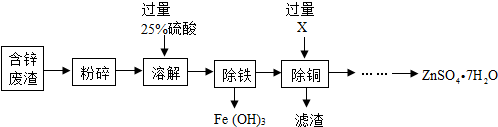
(1)粉碎的目的是加快反应速率,利于充分反应.
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,配制溶液时需要的玻璃仪器有胶头滴管﹑玻璃棒﹑量筒和烧杯.
(3)物质X是锌.
分析 (1)根据含锌废渣粉碎,能增大反应物的接触面积,进行分析解答.
(2)利用浓溶液配制稀溶液,采用的加水稀释的方法,结合题意进行分析解答.
(3)根据加入过量X的目的是除铜,同时得到硫酸锌溶液,进行分析解答.
解答 解:(1)含锌废渣粉碎,能增大反应物的接触面积,能加快反应速率,利于充分反应.
(2)若实验室用质量分数为98%的硫酸配制200g25%的硫酸,采用的加水稀释的方法,操作步骤是计算、量取、混匀,量筒与胶头滴管用于准确量取浓硫酸和水;烧杯用于完成混匀操作、玻璃棒用于混匀时的搅拌.
(3)加入过量X的目的是除铜,同时得到硫酸锌溶液,锌能与硫酸铜溶液反应生成硫酸锌溶液和铜,能分离出铜,同时生成硫酸锌溶液,故X是锌.
故答案为:(1)加快反应速率,利于充分反应;(2)烧杯;(3)锌.
点评 本题难度不大,理解含锌废渣为原料制备七水硫酸锌的反应流程,掌握金属的化学性质、用浓溶液配制配制稀溶液的基本步骤等是正确解答本题的关键.

练习册系列答案
相关题目
16.物质存放在烧杯中一段时间后,质量变大且变质的是( )
①浓盐酸②浓硫酸③烧碱④生石灰⑤澄清石灰水.
①浓盐酸②浓硫酸③烧碱④生石灰⑤澄清石灰水.
| A. | ③④⑤ | B. | ②③④⑤ | C. | ①②③④⑤ | D. | ④⑤ |
17.下列描述完全正确的是( )
| A. | 可用肥皂水区别硬水与软水 | |
| B. | 人体缺乏维生素C会引起夜盲症 | |
| C. | 在化学反应中只有燃烧才能放出热量 | |
| D. | 合成橡胶、合金都属于合成材料 |
7.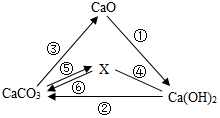 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )| A. | 物质X是一种常见的金属氧化物 | |
| B. | 反应②类型一定属于复分解反应 | |
| C. | 反应①会放出热量,而反应③能耗大 | |
| D. | 向Ca(OH)2溶液中加入CaO固体,所得溶液的溶质质量分数一定会增大 |
1.如表是国家对“饮酒驾车”和“醉酒驾车”的界定标准:
白酒、红酒和啤酒中均含有乙醇(俗称酒精,化学式为C2H5OH),饮酒后酒精可进入人体血液中.请回答下列问题:
(1)乙醇(C2H5OH)中碳、氢、氧元素的质量比是C﹕H﹕O=12:3:8;
(2)饮酒会使人的中枢神经系统过度兴奋或麻痹抑制,容易引发交通事故.某人饮酒后驾车,被交警发现,经测定其每100毫升血液中酒精含量为93毫克,属于醉酒驾车;
(3)在治理酒后驾车中,酒精检测仪发挥了重要作用.如图甲是酒精检测仪,图乙是检测仪的简化电路图,R0为定值电阻,R为气敏电阻,该电阻阻值与酒精气体含量的关系如图丙,如果图乙中电流表示数越大,说明司机吹出的气体中酒精含量就越大.

| 饮酒驾车 | 20毫克/100毫升≤血液中的酒精含量<80毫克/100毫升 |
| 醉酒驾车 | 血液中的酒精含量≥80毫克/100毫升 |
(1)乙醇(C2H5OH)中碳、氢、氧元素的质量比是C﹕H﹕O=12:3:8;
(2)饮酒会使人的中枢神经系统过度兴奋或麻痹抑制,容易引发交通事故.某人饮酒后驾车,被交警发现,经测定其每100毫升血液中酒精含量为93毫克,属于醉酒驾车;
(3)在治理酒后驾车中,酒精检测仪发挥了重要作用.如图甲是酒精检测仪,图乙是检测仪的简化电路图,R0为定值电阻,R为气敏电阻,该电阻阻值与酒精气体含量的关系如图丙,如果图乙中电流表示数越大,说明司机吹出的气体中酒精含量就越大.

 (1)下列是与水有关的几个描述,请根据所学知识填写完整:
(1)下列是与水有关的几个描述,请根据所学知识填写完整: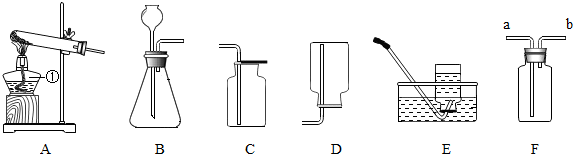
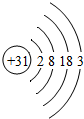 ,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是B(填序号).
,下列原子结构示意图所对应的元素与镓元素的化学性质相似的是B(填序号).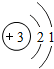 B.
B.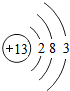 C.
C.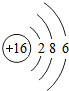 D.
D.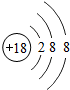
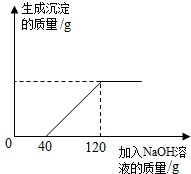 现有含HCl和CuCl2的混合溶液100g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成Cu(OH)2沉淀的质量与加入NaOH溶液的质量关系如图所示.
现有含HCl和CuCl2的混合溶液100g,向该溶液中逐滴加入溶质质量分数为10%的NaOH溶液,生成Cu(OH)2沉淀的质量与加入NaOH溶液的质量关系如图所示.