题目内容
14.判断下列物质组合能发生复分解反应的有①③⑥(填序号)①K2CO3+CaCl2 ②H2SO4+KCl ③CuO+HCl ④Fe+CuSO4 ⑤CO2+NaOH
⑥K2SO4+BaCl2 ⑦Mg(OH)2+CuSO4 ⑧BaCO3+NaOH.
分析 根据复分解反应发生的条件,若两种物质相互交换成分有沉淀、气体或水生成,则能发生化学反应;反应物要求必须是可溶的(当有酸参与反应时,另一种物质可不溶于水,但一定要溶于酸才行,也就是能与酸发生反应),进行分析解答.
解答 解:①K2CO3与CaCl2相互交换成分生成碳酸钙沉淀和氯化钾,能发生复分解反应.
②H2SO4与KCl 相互交换成分没有沉淀、气体或水生成,不能发生复分解反应.
③CuO与HCl 反应生成氯化铜和水,能发生复分解反应.
④Fe与CuSO4反应生成硫酸亚铁和铜,该反应属于置换反应.
⑤CO2与NaOH反应生成碳酸钠和水,该反应不是两种化合物相互交换成分生成两种新的化合物的反应,不属于复分解反应.
⑥K2SO4与BaCl2相互交换成分生成硫酸钡沉淀和氯化钾,能发生复分解反应.
⑦Mg(OH)2难溶于水,不能与CuSO4发生复分解反应.
⑧BaCO3难溶于水,不能与NaOH发生复分解反应.
故答案为:①③⑥.
点评 本题难度不大,掌握复分解反应发生的条件(有沉淀、气体或水生成)并能灵活运用是正确解答本题的关键.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
4.某校化学活动小组开展了一场关于金属镉、铜、银活动性顺序的探究及镉污染事故处理方法的研讨活动.
【查阅资料】①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;②水体中镉元素通常以氯化镉的形式存在;
【提出假设】小组同学对三种金属的活动性顺序提出如下假设:
a.镉>铜>银
b.铜>银>镉
c.铜>镉>银.
【进行实验】
【得出结论】原假设中正确的是a(填“a”“b”或“c”)
【反思与应用】小组同学根据查阅的资料对镉污染事故处理方法进行了如下讨论:
(1)小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为CdCl2+2NaOH=Cd(OH)2↓+2NaCl.
(2)小敏认为该方案虽然有效,但有缺陷,原因是氢氧化钠具有强腐蚀性,因此过量的氢氧化钠会污染环境.受小聪与小敏启发,你认为可以用氢氧化钙代替烧碱.
(3)请重新设计实验来探究镉、铜、银三种金属的活动性顺序
【查阅资料】①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;②水体中镉元素通常以氯化镉的形式存在;
【提出假设】小组同学对三种金属的活动性顺序提出如下假设:
a.镉>铜>银
b.铜>银>镉
c.铜>镉>银.
【进行实验】
| 实验步骤 | 实验现象 |
| 取适量镉、铜、银于不同试管中,分别加入足量稀盐酸. | 镉表面有气泡产生,铜、银表面无气泡产生 |
| 取适量铜于试管中,加入少量硝酸银溶液 | 铜表面盖了一层银白色物质,溶液由无色变为蓝色 |
【反思与应用】小组同学根据查阅的资料对镉污染事故处理方法进行了如下讨论:
(1)小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为CdCl2+2NaOH=Cd(OH)2↓+2NaCl.
(2)小敏认为该方案虽然有效,但有缺陷,原因是氢氧化钠具有强腐蚀性,因此过量的氢氧化钠会污染环境.受小聪与小敏启发,你认为可以用氢氧化钙代替烧碱.
(3)请重新设计实验来探究镉、铜、银三种金属的活动性顺序
| 实验步骤 | 实验现象 | 实验结论 |
5.我市盛产茶叶,“永嘉乌牛早”、“泰顺高山云雾茶”等绿茶享誉海内外.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列关于单宁酸的说法正确的是( )
| A. | 一个单宁酸分子中含23个氧分子 | |
| B. | 单宁酸分子相对分子质量为174 | |
| C. | 单宁酸分子碳氢氧原子个数比为76:52:46 | |
| D. | 单宁酸分子由碳氢氧三种元素组成 |
9. 根据表格回答:部分酸、碱和盐在水中的溶解性(20℃).
根据表格回答:部分酸、碱和盐在水中的溶解性(20℃).
(1)从表中找出一种微溶性盐 CaSO4(填化学式).
(2)现有一包固体粉末,可能是CaCO3、Na2CO3、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
①取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有CaCO3、CuSO4.
②取上述溶液适量,滴加盐酸溶液后产生气泡.则此固体粉末中一定有Na2CO3.
(3)现有盐酸和CaCl2的混合溶液,向其中逐渐加入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X是D.(选填字母编号)
A.水 B.稀盐酸 C.氯化铵溶液 D.纯碱溶液.
 根据表格回答:部分酸、碱和盐在水中的溶解性(20℃).
根据表格回答:部分酸、碱和盐在水中的溶解性(20℃).| 阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Cu2+ | 不 | 溶 | 溶 | 溶 | 不 |
(2)现有一包固体粉末,可能是CaCO3、Na2CO3、CuSO4、NaCl中的一种或几种,为确定其组成,取适量试样进行下列实验.请根据实验现象判断:
①取试样溶于水,得到无色澄清溶液,则此固体粉末中一定没有CaCO3、CuSO4.
②取上述溶液适量,滴加盐酸溶液后产生气泡.则此固体粉末中一定有Na2CO3.
(3)现有盐酸和CaCl2的混合溶液,向其中逐渐加入过量的某物质X,溶液的pH随滴入X的量的变化关系如图所示,则X是D.(选填字母编号)
A.水 B.稀盐酸 C.氯化铵溶液 D.纯碱溶液.
6.下列物质在敞口容器中放置一段时间后,会发生反应且质量会增加的是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 氢氧化钠 | D. | 食盐水 |
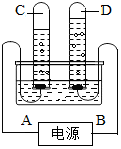 水是我们生活中重要物质.请用学过的知识回答下列有关问题:
水是我们生活中重要物质.请用学过的知识回答下列有关问题: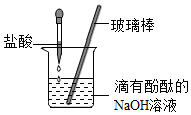 盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中科学许多实验都用到了盐酸.
盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中科学许多实验都用到了盐酸.