题目内容
4.如果人体血液中缺乏亚铁离子,就会造成“贫血”.市场出售的某种麦片中含有微量的颗 粒很细的还原铁粉.这种铁粉在人体胃液(主要成份为稀盐酸)中转化为亚铁盐的化学方程式是Fe+2HCl═FeCl2+H2↑.分析 根据题意,还原铁粉与胃液的主要成份盐酸反应生成氯化亚铁溶液和氢气,写出反应的化学方程式即可.
解答 解:还原铁粉与胃液的主要成份盐酸反应生成氯化亚铁溶液和氢气,反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
故答案为:Fe+2HCl═FeCl2+H2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
15.下类物质不能用来鉴别稀硫酸和氢氧化钠溶液的是( )
| A. | 碳酸钠溶液 | B. | 硫酸铜溶液 | C. | 石蕊试液 | D. | 硫酸钠溶液 |
19.如图两圆相交部分是五种物质中两两之间相互反应的示意图.下列对反应现象的说法中,错误的是( )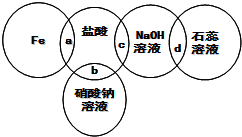

| A. | a处形成浅绿色溶液 | B. | b处形成大量气泡 | ||
| C. | c处反应放热 | D. | d处溶液呈蓝色 |
5.某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液加入稀盐酸一会后,发现忘记了滴加指示剂.因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;
猜想二:可能只有CaCl2;
猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)随着大家环保意识的增强,实验室产生的污染越来越受到重视,实验中产生的污染物必须无害化处理后再排放.要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的碳酸钙.
【提出问题】该烧杯内溶液中的溶质是什么?
【猜想】猜想一:可能是CaCl2和Ca(OH)2;
猜想二:可能只有CaCl2;
猜想三:可能是CaCl2和HCl.
【查阅资料】氯化钙溶液呈中性.
【方案设计】
| 方案 | 方法步骤 | 实验现象 | 实验结论 |
| 方案一 | 取少量烧杯内的溶液于试管中,滴入几滴无色酚酞溶液 | 溶液不变红色 | 猜想一不正确 |
| 方案二 | 取少量烧杯内的溶液于试管中,逐滴加入碳酸钠溶液至过量 | 溶液变红色 | 猜想二不正确猜想三正确 |
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
(2)随着大家环保意识的增强,实验室产生的污染越来越受到重视,实验中产生的污染物必须无害化处理后再排放.要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的碳酸钙.
2.氧气是我们身边常见的物质,以下关于氧气的叙述不正确的是( )
| A. | 物质与氧气发生的反应都是氧化反应 | |
| B. | 氧气能使带火星的木条复燃 | |
| C. | 鱼、虾能在水中生存是由于氧气易溶于水 | |
| D. | 氧气可以供给呼吸,和体内物质反应而释放能量,维持生命活动 |
3.同学们对生活、生产中一些做法的解释不合理的是( )
| A. | 用洗发剂、洗面奶可以洗去油污,因为它们具有乳化功能 | |
| B. | 若铵态氮肥和碱性物质混合施用,会降低铵态氮肥的肥效 | |
| C. | 软质铅笔芯的粉末灌入生锈的锁孔里比较容易打开,是因为减小了摩擦 | |
| D. | 菜刀刀口磨得很锋利,是为了增大压力 |
 ;
;