题目内容
2.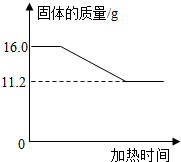 先称取一定质量的氯酸钾和二氧化锰混合物、放入大试管中加热至质量不再变化为止.实验测得固体混合物质量随加热时间变化的相关数据如图所示.请计算
先称取一定质量的氯酸钾和二氧化锰混合物、放入大试管中加热至质量不再变化为止.实验测得固体混合物质量随加热时间变化的相关数据如图所示.请计算(1)产生氧气的质量为多少?
(2)原混合物中氯酸钾的质量?
分析 从图象中可以看出固体的质量在反应前后减少了,结合反应可知减少的质量即为气体的质量,可以据此求算.
解答 解:(1)由固体质量减少的即为氧气的质量,可知生成氧气的质量为:16.0g-11.2g=4.8g;
(2)设原混合物中氯酸钾的质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
x 4.8g
$\frac{245}{x}=\frac{96}{4.8g}$
解得:x=12.25g
答:(1)生成氧气是4.8g克;(2)求原混合物中氯酸钾的质量是12.25g.
点评 主要考查了根据化学方程式进行相关的计算及质量守恒定律的应用,培养学生的应用知识的能力和解决问题的能力,要注意根据题给的数据进行分析得出已知量作为解题的依据.

练习册系列答案
相关题目
12.下列反应中属于化合反应的是( )
| A. | 氧化汞$\stackrel{加热}{→}$ 汞+氧气 | B. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | ||
| C. | 硫+氧气$\stackrel{点燃}{→}$ 二氧化硫 | D. | 石蜡+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
7.08年月我国北京成功举办了以“绿色奥运”为理念的运动会,北京的空气质量倍受人们的关注.下列物质中,未计入北京市监测空气污染指数项目的是( )
| A. | 二氧化硫 | B. | 一氧化碳 | C. | 可吸入的颗粒物 | D. | 氮气 |
11.用物质的名称或化学式填写表:
| 名称 | 3个亚铁离子 | 氯化铵 | 硝酸锌 | 葡萄糖 | 氢氧化铜 |
| 化学式 | 3Fe2+ | NH4Cl | Zn(NO3)2 | C6H12O6 | Cu(OH)2 |
9.如图是某化学反应的示意图( )


| A. | 氢气的燃烧 | B. | 水的电解 | C. | 甲烷的燃烧 | D. | 一氧化碳的燃烧 |
 如图是铁丝在氧气中燃烧的实验,回答下列问题:
如图是铁丝在氧气中燃烧的实验,回答下列问题: