题目内容
9.如图是实验室提供的常用仪器,供完成下列气体制取实验时选用(不可重复选用).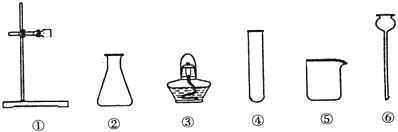
(1)仪器①的名称是:铁架台仪器②的名称是:锥形瓶
(2)实验室采用加热高锰酸钾晶体制取氧气时,其发生装置必须选用上述仪器中的(填序号)①③④,还缺少的仪器是集气瓶.反应的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,,该反应的反应类型为分解反应.
(3)过氧化氢(H2O2)俗称双氧水,常温下是一种无色液体,它在土豆块的催化作用下能迅速分解,放出氧气.若实验室采用该反应原理制取氧气,并且在实验过程中可以随时添加双氧水,上述仪器中必须使用的有②⑥;
(4)把上面分解KMnO4制取氧气的仪器装配好后,检验该装置气密性的操作方法为:把导管一端浸入水中,然后双手紧握试管,观察到有气泡产生,装置气密性良好.
分析 据图即可知道仪器的名称,根据制取装置需要的仪器进行分析解答;加热高锰酸钾分解生成的是锰酸钾、二氧化锰和氧气,根据检查装置气密性的方法解答即可.
解答 解:(1)据图可以看出,仪器①是铁架台,仪器②是锥形瓶,故填:铁架台,锥形瓶;
(2)实验室采用加热高锰酸钾晶体制取氧气时,是固体加热型反应,其发生装置必须选用上述仪器中的铁架台、酒精灯、试管,还缺少集气瓶.加热高锰酸钾分解生成的是锰酸钾、二氧化锰和氧气,反应的文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,该反应属于分解反应,故填:①③④,集气瓶,高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气,分解反应.
(3)若实验室采用过氧化氢制取氧气,是固液常温型反应,在实验过程中可以随时添加双氧水,上述仪器中必须使用的有锥形瓶和长颈漏斗,故填:②⑥;
(4)将分解KMnO4制取氧气的仪器装配好后,检验该装置气密性的操作方法为:把导管一端浸入水中,然后双手紧握试管,观察到有气泡产生,装置气密性良好,故填:把导管一端浸入水中,然后双手紧握试管,观察到有气泡产生,装置气密性良好.
点评 本题考查的是常见气体的实验室制取的知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
2.央视《舌尖上的中国》节目的热播,让厨房再次成为人们施展厨艺的舞台,其实厨房也是同学们的家庭实验室.利用厨房中的物品不可以进行的实验是( )
| A. | 探究铁制品在什么条件下生锈 | |
| B. | 比较不同物质在水中的溶解能力 | |
| C. | 用燃着的火柴检查天然气管道是否漏气 | |
| D. | 探究影响液体蒸发快慢的因素 |
4.同学们整理实验室时,发现一瓶白色固体粉末状药品.实验老师告诉大家药品可能是碳酸钠、碳酸钙、氯化钠、氢氧化钠、硫酸钡中的一种或几种.同学们对此很好奇,于是他们对这瓶白色粉末的成分做了如下探究.
【实验I】小伟取一定量白色粉末于烧杯中,加足量水搅拌,过滤,得到固体和无色滤液.
【实验II】小伟取少量实验I得到的无色滤液于试管中,滴加无色酚酞后,观察到变成红色.于是小伟马上就得出结论,该瓶白色粉末一定有氢氧化钠.但是小旭却认为小伟的结论不一定正确,你认为小旭的理由是(1)碳酸钠的溶液也为碱性.于是小旭另取少量滤液于试管中,加入过量氯化钡溶液,有白色沉淀产生;取上层清液,加入少量氯化铁溶液产生红褐色沉淀.
根据现象,你认为滤液中的溶质有(2)NaOH、Na2CO3,(填化学式,下同)请用相关化学方程式解释这些现象(3)BaCl2+Na2CO3=BaCO3↓+2NaCl;
3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
【实验III】小伟和小旭认为有必要再对实验I中滤渣的成分进行探究,过程如下:
【交流】实验结束后,同学们一致认为通过实验Ⅱ能确定原试剂瓶中还含有(4)NaOH、Na2CO3,但小伟和小旭同学认为,通过上述实验还是不能证明原瓶中是否含有(5NaCl.
【实验I】小伟取一定量白色粉末于烧杯中,加足量水搅拌,过滤,得到固体和无色滤液.
【实验II】小伟取少量实验I得到的无色滤液于试管中,滴加无色酚酞后,观察到变成红色.于是小伟马上就得出结论,该瓶白色粉末一定有氢氧化钠.但是小旭却认为小伟的结论不一定正确,你认为小旭的理由是(1)碳酸钠的溶液也为碱性.于是小旭另取少量滤液于试管中,加入过量氯化钡溶液,有白色沉淀产生;取上层清液,加入少量氯化铁溶液产生红褐色沉淀.
根据现象,你认为滤液中的溶质有(2)NaOH、Na2CO3,(填化学式,下同)请用相关化学方程式解释这些现象(3)BaCl2+Na2CO3=BaCO3↓+2NaCl;
3NaOH+FeCl3═Fe(OH)3↓+3NaCl.
【实验III】小伟和小旭认为有必要再对实验I中滤渣的成分进行探究,过程如下:
| 步骤 | 实验现象 |
| (1)取少量液于试管,向其滴加足量稀盐酸溶液,振荡 | 有气体冒出,试管底还残留少量固体 |
| (2)过滤,取少量滤液于试管中,加入硝酸银和稀硝酸溶液 | 有白色沉淀生成 |
1. 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式:4Al+3O2=2Al2O3.
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是B(填字母).
A.产生的气体可能是H2 B.产生的气体可能是CO2
C.CuSO4溶液中可能含有少量的某种酸 D.CuSO4溶液的pH可能小于7
(3)某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”.某研究性学习小组对该厂生产的烧碱样品进行如下研究.
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想一:可能含有Na2CO3.作出此猜想的依据是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl.作出此猜想的依据是可能有少量的氯化钠没有反应(用简洁的文字表示).
【实验设计】
(4)某同学取100g含有H2SO4的酸性废水,然后滴加烧碱溶液中和,至溶液pH=7时,共消耗质量分数为20%的烧碱溶液20g.求这种废水中含H2SO4的质量分数.
 元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.
元素化合物知识是初中化学重要的学习内容.请回答下列有关元素化合物的问题.(1)根据如图信息,写出甲、乙两种元素的单质间发生反应的化学方程式:4Al+3O2=2Al2O3.
(2)某同学将铁片放入CuSO4溶液中,发现铁片表面有红色物质析出,同时还有少量无色无味气泡产生.对于产生气泡的“异常现象”,下列猜想不合理的是B(填字母).
A.产生的气体可能是H2 B.产生的气体可能是CO2
C.CuSO4溶液中可能含有少量的某种酸 D.CuSO4溶液的pH可能小于7
(3)某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方程式:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”.某研究性学习小组对该厂生产的烧碱样品进行如下研究.
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】
猜想一:可能含有Na2CO3.作出此猜想的依据是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl.作出此猜想的依据是可能有少量的氯化钠没有反应(用简洁的文字表示).
【实验设计】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁试 | 管外壁发热 | 原因是氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体 | 样品中含有的杂质是碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还还有的杂质是氯化钠 |
18.下列有关说法或实验方法不合理的是( )
| A. | “缺铁性贫血”里所说的铁不是单质铁 | |
| B. | 家用铝锅不可以用来盛放酸性食物 | |
| C. | 水可用来鉴别硝酸钾固体和氢氧化钠固体 | |
| D. | 铁丝和铜丝分别插入氢氧化钠溶液中,都无变化,说明铁和铜一样不活泼 |

