题目内容
补全化学方程式:
(1) C3H8+ O2═ CO2+ H2O
(2) N2H4+ N2O4═ N2+ H2O
(3) FeS2+ O2═ Fe2O3+ SO2
(4) Na+ H2O═ NaOH+ H2↑
(5) Al+ HCl═ AlCl3+ H2↑
(6) Fe2O3+ CO═ Fe+ CO2
(7) CO+ Fe3O4═ Fe+ CO2.
(1)
(2)
(3)
(4)
(5)
(6)
(7)
考点:化学方程式的配平
专题:化学用语和质量守恒定律
分析:依据质量守恒定律:反应前后原子的种类和数目不变,结合具体化学反应特点利用不同的方法进行配平.
解答:解:(1)利用‘定一法’,把最复杂的化合物的计量数,即C3H8的计量数设为1,然后配二氧化碳中碳原子、水中氢原子,最后再配平氧原子,计量数分别为:1 5 3 4;
(2)利用‘最小公倍数’法,以N2O4为起点先配平氧原子,然后配平氢原子,最后配平氮原子,计量数分别为:2 1 3 4;
(3)利用‘奇数配偶法’先在Fe2O3前配2,将氧原子个数化为偶数,然后配平铁原子,进而配平硫原子,最后配平氧原子,计量数分别为:4 11 2 8;
(4)利用‘奇数配偶法’先在NaOH前配2,将氧原子个数化为偶数,然后配平氧原子、钠原子,最后配平氢原子,计量数分别为:2 2 2 1;
(5)利用‘奇数配偶法’先在AlCl3前配2,将氯原子个数化为偶数,然后配平氯原子、铝原子,再配平氢原子,计量数分别为:2 6 2 3;
(6)观察方程式可知:每个一氧化碳分子得到1个氧原子变为二氧化碳分子,每个Fe2O3分子含有3个氧原子,则需要3个一氧化碳分子来还原,即一氧化碳还原金属氧化物时,一氧化碳的计量数等于氧化物中氧原子的个数,计量数分别为:1 3 2 3;
(7)由(6)分析可知:一氧化碳的计量数和每个Fe3O4分子中氧原子的数目相同,是4,计量数分别为:4 1 3 4;
故答案为:(1)1 5 3 4;
(2)2 1 3 4;
(3)4 11 2 8;
(4)2 2 2 1;
(5)2 6 2 3;
(6)1 3 2 3;
(7)4 1 3 4.
(2)利用‘最小公倍数’法,以N2O4为起点先配平氧原子,然后配平氢原子,最后配平氮原子,计量数分别为:2 1 3 4;
(3)利用‘奇数配偶法’先在Fe2O3前配2,将氧原子个数化为偶数,然后配平铁原子,进而配平硫原子,最后配平氧原子,计量数分别为:4 11 2 8;
(4)利用‘奇数配偶法’先在NaOH前配2,将氧原子个数化为偶数,然后配平氧原子、钠原子,最后配平氢原子,计量数分别为:2 2 2 1;
(5)利用‘奇数配偶法’先在AlCl3前配2,将氯原子个数化为偶数,然后配平氯原子、铝原子,再配平氢原子,计量数分别为:2 6 2 3;
(6)观察方程式可知:每个一氧化碳分子得到1个氧原子变为二氧化碳分子,每个Fe2O3分子含有3个氧原子,则需要3个一氧化碳分子来还原,即一氧化碳还原金属氧化物时,一氧化碳的计量数等于氧化物中氧原子的个数,计量数分别为:1 3 2 3;
(7)由(6)分析可知:一氧化碳的计量数和每个Fe3O4分子中氧原子的数目相同,是4,计量数分别为:4 1 3 4;
故答案为:(1)1 5 3 4;
(2)2 1 3 4;
(3)4 11 2 8;
(4)2 2 2 1;
(5)2 6 2 3;
(6)1 3 2 3;
(7)4 1 3 4.
点评:本题考查了方程式的配平,可根据具体化学反应方程式采取不同的方法进行配平.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
水是生命之源.下列各种“水”属于纯净物的是( )
| A、矿泉水 | B、糖水 |
| C、蒸馏水 | D、澄清石灰水 |
实验室用KMnO4加热制取氧气的主要操作步骤为:①把KMnO4放入试管内,塞上带导管的塞子 ②检查装置的气密性 ③给试管加热 ④用排水法收集氧气 ⑤熄灭酒精灯停止加热 ⑥从水槽中取出导气管.其中操作顺序前后排列正确的是( )
| A、①②③④⑤⑥ |
| B、②①③④⑤⑥ |
| C、③②①④⑥⑤ |
| D、②①③④⑥⑤ |
下列试验操作中,“先”与“后”的顺序不正确的是( )
| A、制备气体时,先检查装置的气密性,后装药品 |
| B、用试管加热时,先使试管底部均匀受热,后用酒精灯的外焰固定加热 |
| C、用量筒量取40mL液体时,先倒入接近40mL的液体,后用胶头滴管补至刻度线 |
| D、用托盘天平称量物质时,先加质量小的砝码,再加质量大的砝码,最后移动游码 |
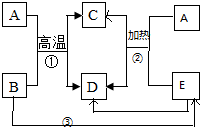 已知A~E是常见的五种物质,存在如图所示的转化关系,其中C是红色金属单质,D能使澄清石灰水变浑浊.请回答下列问题:
已知A~E是常见的五种物质,存在如图所示的转化关系,其中C是红色金属单质,D能使澄清石灰水变浑浊.请回答下列问题:
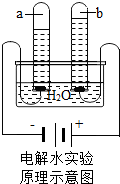 如图所示是电解水实验装置,通电一段时间后,在两个试管中分别收集到气体a和b,请回答:
如图所示是电解水实验装置,通电一段时间后,在两个试管中分别收集到气体a和b,请回答: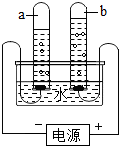 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: