题目内容
10.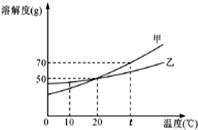 小明绘制的两种固体物质的溶解度曲线如图所示:
小明绘制的两种固体物质的溶解度曲线如图所示:(1)t℃时,甲物质的溶解度为70g.
(2)20℃时,甲的溶解度=(<、>或=)乙的溶解度.
(3)当温度为小于20℃,乙的溶解度大于甲;当温度为大于20℃,甲的溶解度大于乙.
(4)现有一瓶甲的饱和溶液,如果要使之变为不饱和溶液,可以采用的方法BC.
A、降低温度 B、升高温度 C、增加溶剂 D、蒸发溶剂.
分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;t℃时,甲物质的溶解度为70g;20℃时,甲的溶解度等于乙的溶解度;当温度为小于20℃,乙的溶解度大于甲;当温度为大于20℃,甲的溶解度大于乙;现有一瓶甲的饱和溶液,如果要使之变为不饱和溶液,可以采用的方法是:升高温度、增加溶剂、减少溶质.
解答 解:(1)由溶解度曲线可知:t℃时,甲物质的溶解度为70g;故答案为:
(2)20℃时,甲的溶解度等于乙的溶解度,故答案为:=;
(3)当温度为小于20℃,乙的溶解度大于甲;当温度为大于20℃,甲的溶解度大于乙,故答案为:小于20;大于20;
(4)现有一瓶甲的饱和溶液,如果要使之变为不饱和溶液,可以采用的方法是:升高温度、增加溶剂、减少溶质;故答案为:BC;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关饱和溶液与不饱和溶液的转化方法等,本考点主要出现在选择题和填空题中.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
3.关于水的认识正确的是( )
| A. | 电解水得到氢气和氧气,则水由氢原子和氧原子构成 | |
| B. | 生活中用过滤的方法可以降低水的硬度 | |
| C. | 净化水的方法有沉淀、过滤、吸附和蒸馏等 | |
| D. | 汽油、蔗糖加入一定量水中都能形成溶液 |
1.某同学的化学实验报告中有如下记录,其中合理的是( )
| A. | 用10毫升量筒量取8.2毫升稀硫酸溶液 | |
| B. | 用水银温度计测得某溶液的温度为20.54℃ | |
| C. | 用pH试纸测得某浓硫酸的pH值为1 | |
| D. | 用托盘天平称取17.14克氯化钠固体 |
18.下列化学方程式书写和反应类型标注都正确的是( )
| A. | CuO+CO═Cu+CO2↑ (置换反应) | |
| B. | 2KClO3 MnO2 $\frac{\underline{\;MnO_2\;}}{\;}$2KCl+3O2↑(分解反应) | |
| C. | CuSO4+Ba(OH)2═Cu(OH)2↓+BaSO4↓(复分解反应) | |
| D. | Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$MgO2 (化合反应) |
15.下列生产、生活中的做法正确的是( )
| A. | 用钢刷来擦洗铝制品 | |
| B. | 一氧化碳还原氧化铜后,沾在试管壁上的紫红色固体物质,可以用稀盐酸除去 | |
| C. | 汽车修理工用汽油洗涤衣服上的油污 | |
| D. | 为防止被雨水淋湿的自行车生锈,应先用油布擦,再用干布擦净 |
2.我国铁路将进入高铁时代.为适应提速要求需把短轨焊接连成长轨,常用反应:xAl+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+xFe进行焊接,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作.下列说法不正确的是( )
| A. | 该反应为置换反应 | B. | 该反应会放出大量热 | ||
| C. | Fe2O3为氧化物 | D. | 该反应方程式中的x为3 |
20.知Cn的相对原子质量为277,其质子数是112,则这种原子的核外电子数为( )
| A. | 112 | B. | 165 | C. | 277 | D. | 389 |
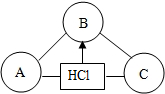 构建知识网络是一种重要的学习方法.右图是关于盐酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.
构建知识网络是一种重要的学习方法.右图是关于盐酸化学性质的知识网络,“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.