题目内容
4.把H2通过2g加热的赤铁矿粉(主要成分是Fe2O3,其它杂质不参加反应,3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O),待反应完毕后,测得固体净重1.52g,问能生成多少克的单质铁?分析 由反应后固体物质的质量、赤铁矿石的质量,根据一氧化碳与氧化铁反应的化学方程式,采用量差法可以对相关问题进行解答
解答 解:设生成的铁的质量是x
3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 固质量减轻
160 112 160-112=48
x 2g-1.52g=0.48g
$\frac{112}{x}$=$\frac{48}{0.48g}$
解得x=11.2g
答:能生成11.2克的单质铁.
点评 本题考查学生利用化学反应方程式的计算,容易将习题中的数据直接代入计算而出错,注意一题多解,并注意差量法是解答此类习题较好较快的方法,学生应熟练掌握.

练习册系列答案
相关题目
15.下列关于催化剂说法正确的是( )
| A. | 催化剂一定会加快反应的速率 | |
| B. | 在高锰酸钾制取氧气的反应中,二氧化锰属于反应的催化剂 | |
| C. | 催化剂在化学反应中本身的性质和质量保持不变 | |
| D. | 在化学变化中质量和化学性质不变的物质不一定是催化剂 |
12.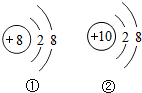 从如图所示的两种微观示意图中,所获取信息不正确的是( )
从如图所示的两种微观示意图中,所获取信息不正确的是( )
 从如图所示的两种微观示意图中,所获取信息不正确的是( )
从如图所示的两种微观示意图中,所获取信息不正确的是( )| A. | 它们都表示稀有气体元素的原子 | B. | 它们的核外电子层数相同 | ||
| C. | 它们属于不同种元素 | D. | ①表示阴离子,②表示原子 |
9.2014年8月12日,李克强总理批示,抓好东北等粮食主产区的抗旱保秋工作,确保群众饮水安全.干旱地区工业生产中采取的下列措施中不合理的是( )
| A. | 改漫灌为滴灌或喷灌 | B. | 抽取地下水灌溉 | ||
| C. | 直接用工厂废水浇灌农作物 | D. | 因地制宜,选种耐旱能力强的作物 |
14.下列化学现象的描述正确的是( )
| A. | 红磷在空气中燃烧,产生大量的白雾 | |
| B. | 铁丝在空气中燃烧,火星四射,生成一片白色固体 | |
| C. | 木炭在氧气中燃烧比在空气中燃烧旺,发出白光,并放出热量 | |
| D. | 硫在空气中燃烧发出明亮的蓝紫色的火焰 |
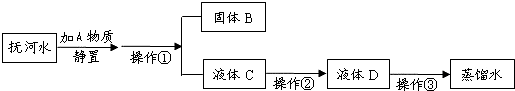
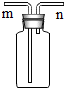 阅读材料回答问题.
阅读材料回答问题.