题目内容
2.一定质量的碳酸钠和氯化钠固体混合物,加入101克水完全溶解后,再往其中加入100g氯化钙溶液,恰好完全反应.过滤,将滤渣干燥,称得其质量为10g,测得滤液中溶质的质量分数为10%.试计算:(1)100g氯化钙溶液中溶质的质量;
(2)原固体混合物中碳酸钠的质量分数.
分析 (1)根据氯化钠、碳酸钠的性质,氯化钠不能与加入的氯化钙发生反应.碳酸钠与氯化钙生成碳酸钙沉淀和氯化钠,根据生成沉淀碳酸钙的质量可计算氯化钙溶液中溶质的质量,
(2)结合题给的条件可以求算出滤液中氯化钠的质量,再求出原混合物中氯化钠的质量,最后即可求出纯碱样品中碳酸钠的质量分数.
解答 解:(1)设恰好完全反应时参加反应的碳酸钠的质量为x,氯化钙溶液中氯化钙的质量为y,生成氯化钠的质量为Z,
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 111 100 117
x y 10g Z
$\frac{106}{x}$=$\frac{111}{y}$=$\frac{100}{10g}$=$\frac{117}{z}$
解得:X=10.6g y=11.1g Z=11.7g
(2)由题意可知,设原混合物中氯化钠的质量为a,则
$\frac{a+11.7g}{10.6g+a+101g+100g-10g}$×100%=10%
解得:a=9.4g
纯碱样品中碳酸钠的质量分数为:$\frac{10.6g}{9.4g+10.6g}$×100%=53%
答:(1)氯化钙溶液中溶质的质量为11.1g;(2)纯碱样品中碳酸钠的质量分数为53%.
点评 在解答本题一定要注意,滤液的质量不是100g+101g-10g=211g,否则计算出的滤液中氯化钠的质量小于生成的氯化钠的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.水是生命之源,下列有关水的说法正确的是( )
| A. | 节约用水和防治水体污染是爱护水资源的有效途径 | |
| B. | 水是由氢气和氧气组成的混合物 | |
| C. | 自来水厂净水过程中所采用的方法包括:沉淀、吸附、蒸馏 | |
| D. | 长期饮用纯净水有益身体健康 |
10.学校禁止吸烟,是因为燃着的香烟产生的烟气有害学生健康,其中含有一种能与血液中血红蛋白结合的有毒气体,它是( )
| A. | CO2 | B. | CO | C. | N2 | D. | SO2 |
14.下列是“一定溶质质量分数的氯化钠溶液的配制”的实验操作示意图,其中错误的是( )
| A. | 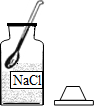 取用氯化钠固体 | B. | 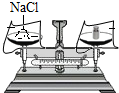 称量氯化钠固体 | C. | 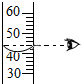 量取水的体积 | D. | 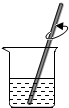 溶解 |
11.正确的实验操作是科学探究成功的基础,下列操作中错误的是( )
| A. | 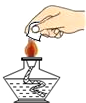 熄灭酒精灯 | B. | 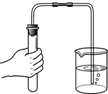 检查气密性 | C. |  滴加液体 | D. | 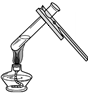 加热液体 |
 化学与生活息息相关,请用学过的化学知识解决下列问题:
化学与生活息息相关,请用学过的化学知识解决下列问题: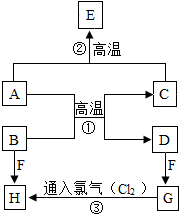 A〜H是初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G-H发生的是化合反应.它们的转化关系如图所示,请回答下列问题:
A〜H是初中化学常见的物质,已知A为黑色固体单质,B为红色粉末,C和E常温下为气体且均属氧化物,F的浓溶液能挥发出剌激性气味的气体,G-H发生的是化合反应.它们的转化关系如图所示,请回答下列问题: 胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g.某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图所示抑酸剂,发生反应:Mg(OH)2+2HCl=MgCl2+2H2O.请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是多少克?理论上能否使该患者胃液中盐酸溶质质量恢复到正常范围?(写出计算过程,结果精确到0.001)
胃酸主要成分是盐酸,正常人胃液每日需要盐酸溶质质量约为6.5g~7.3g.某患者每日分泌盐酸溶质质量为9.0g,为治疗胃酸过多需服用图所示抑酸剂,发生反应:Mg(OH)2+2HCl=MgCl2+2H2O.请计算并回答:按说明书用法用量,每天最多可中和胃液中盐酸溶质质量是多少克?理论上能否使该患者胃液中盐酸溶质质量恢复到正常范围?(写出计算过程,结果精确到0.001)