题目内容
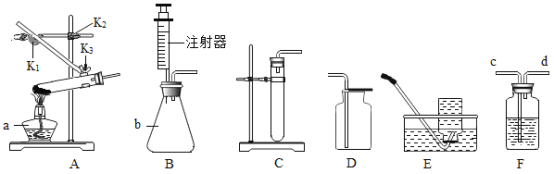
【题目】探究空气中氧气含量的实验(如图所示),回答下列问题:
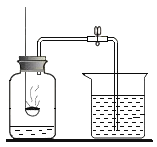
(1)甲同学点燃燃烧匙中的红磷,观察到红磷燃烧,放热,并产生大量的____________________, 该反应的符号表达式____________________。冷却后,打开弹簧夹,出现_________________________的现象。
(2)乙同学用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是________________________。(要求答出一种)
(3)实验结束后,集气瓶中剩余的气体主要是氮气,且瓶内水面上升到一定高度后不 再上升了,由此分析说明,氮气具有的一条性质:_______________________。
(4)丙同学探究能否用镁条代替红磷,将镁条点燃后迅速伸入盛有氮气的集气瓶中,发现镁条剧烈燃烧,发出白光,放热,产生一种叫氮化镁的粉末。请写出镁在氮气中 燃烧反应的文字表达式__________________,分析后认为________ (填“能”或“不能”)代替红磷,原因是________________。若用镁代替红磷实验,进入瓶中水的体积会_______________________(填>或<或=)瓶内空气体积的1/5.
(5)下列有关测定空气中氧气含量实验说法正确的是______________________(填字母).
A 燃烧匙中的红磷越多,水位上升越高
B 本实验可以证明空气含有N2、O2、CO2和稀有气体
C 选用红磷是因为只能与空气中的氧气反应,且生成物为固体
D 集气瓶中先装入少量水是为了吸收生成物,防止污染空气
【答案】白烟 P+O2![]() P2O5 水被倒吸入集气瓶中,约占原水面以上气体体积的五分之一; 装置漏气或红磷的量不足或没有冷却就读数; 氮气既不能燃烧,也不能支持燃烧;或氮气与磷不反应;或氮气难溶于水等; 镁+氮气
P2O5 水被倒吸入集气瓶中,约占原水面以上气体体积的五分之一; 装置漏气或红磷的量不足或没有冷却就读数; 氮气既不能燃烧,也不能支持燃烧;或氮气与磷不反应;或氮气难溶于水等; 镁+氮气![]() 氮化镁, 不能 镁在点燃的条件下,不仅与氧气反应,也与氮气反应 > CD
氮化镁, 不能 镁在点燃的条件下,不仅与氧气反应,也与氮气反应 > CD
【解析】
(1)甲同学点燃燃烧匙中的红磷,观察到红磷燃烧,放热,并产生大量的白烟,即磷和氧气在点燃的条件下生成五氧化二磷,该反应的符号表达式为: P+O2![]() P2O5;氧气被消耗,使密闭容器中压强变小,冷却后,打开弹簧夹,出现的现象是:水被倒吸入集气瓶中,约占原水面以上气体体积的五分之一;
P2O5;氧气被消耗,使密闭容器中压强变小,冷却后,打开弹簧夹,出现的现象是:水被倒吸入集气瓶中,约占原水面以上气体体积的五分之一;
水被倒吸入集气瓶中,约占原水面以上气体体积的五分之一;
(2)乙同学用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是:装置漏气、红磷的量不足、没有冷却就读数;故答案为:装置漏气或红磷的量不足或没有冷却就读数;
(3)根据该实验可知,氮气具有的性质是:氮气既不能燃烧,也不能支持燃烧;氮气与磷不反应;氮气难溶于水等;
(4)镁和氮气在点燃的条件下生成氮化镁,燃烧反应的文字表达式:镁+氮气![]() 氮化镁,分析可知:镁不能代替红磷,原因是:镁在点燃的条件下,不仅与氧气反应,也与氮气反应;若用镁代替红磷实验,进入瓶中水的体积会大于瓶内空气体积的
氮化镁,分析可知:镁不能代替红磷,原因是:镁在点燃的条件下,不仅与氧气反应,也与氮气反应;若用镁代替红磷实验,进入瓶中水的体积会大于瓶内空气体积的![]() ;
;
(5)A、集气瓶中的氧气的量是一定的,反应需要的红磷的量也是一定的,最终进入集气瓶中的水也是一定的,并不是燃烧匙中的红磷越多,水位上升越高,故选项错误;
B、本实验可以证明空气中氧气的含量,但是不能证明空气中含有氮气、氧气、二氧化碳和稀有气体等,故选项错误;
C、选用红磷是因为反应可以耗尽氧气,生成固态的五氧化二磷,故选项正确;
D、集气瓶底部有少量水,既能吸收反应的生成物,又可以防止空气污染,故选项正确。故选CD。

 阅读快车系列答案
阅读快车系列答案【题目】某兴趣小组同学利用如图装置进行相关实验
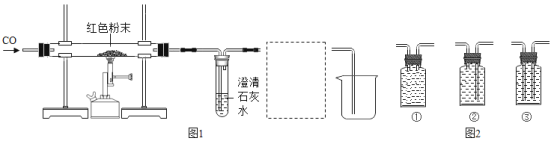
(实验1)模拟炼铁实验
(1)若样品为氧化铁,则A中的实验现象是___________,反应的化学方程式是_____,B中反应的化学方程式是_________。
(2)实验时要先通CO再加热的目的是___________。
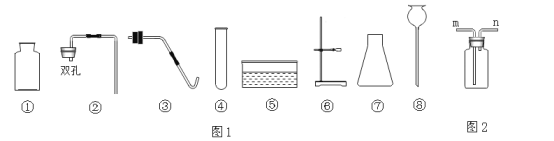
(3)图1虚线框内的装置用于吸收CO2并收集CO,从图2(瓶内均为氢氧化钠溶液)中选择最合适的装置为___________(填序号)。
(实验2)测定样品的组成
若样品有氧化铁、氧化亚铁和四氧化三铁中的一种或几种组成,带充分反应后,实验数据记录如下:
样品质量 | 装置A中玻璃管和固体的总质量 | 装置B的质量 |
2.32g | 反应前55.72g | 反应前281.00g |
反应后55.08g | 反应后281.56g |
样品中铁元素和氧元素的质量比为____________。