题目内容
14.甲、乙、丙三位同学分别取铁粉和铜粉的均匀混合物与某稀硫酸完全反应,所得数据如表:| 甲 | 乙 | 丙 | |
| 金属混合物质量(g) | 10 | 10 | 20 |
| 稀硫酸质量(g) | 100 | 120 | 100 |
| 反应后,过滤得干燥固体质量(g) | 4.4 | 4.4 | 14.4 |
(1)金属混合物中铁的质量分数56%.
(2)该稀硫酸中溶质的质量分数?
分析 由甲和乙对比可知,乙中稀硫酸过量,由甲和丙对比可知,丙中混合物过量,因此甲中铁和稀硫酸恰好完全反应,铁和稀硫酸反应生成硫酸亚铁和氢气,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:由甲和乙对比可知,乙中稀硫酸过量,由甲和丙对比可知,丙中混合物过量,因此甲中铁和稀硫酸恰好完全反应,因此应该用甲中数据进行计算:
(1)甲中反应后,过滤得干燥固体质量是铜的质量,即铜的质量是4.4g,则金属混合物中铁的质量质量为:10g-4.4g=5.6g,
金属混合物中铁的质量分数为:$\frac{5.6g}{10g}$×100%=56%,
故填:56%.
(2)设甲中硫酸质量为x,
Fe+H2SO4=FeSO4+H2↑,
56 98
5.6g x
$\frac{56}{5.6g}$=$\frac{98}{x}$,
x=9.8g,
该稀硫酸中溶质的质量分数为:$\frac{98g.}{100g}$×100%=9.8%,
答:该稀硫酸中溶质的质量分数为9.8%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
4.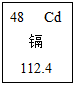 镉是一种重金属元素,在冶金、塑料、电子等行业非常重要.它通常通过废水排入环境中,再通过灌溉进入食物,水稻是典型的“受害作物”,食用后对人体有害.如图,下列有关镉的说法错误的是( )
镉是一种重金属元素,在冶金、塑料、电子等行业非常重要.它通常通过废水排入环境中,再通过灌溉进入食物,水稻是典型的“受害作物”,食用后对人体有害.如图,下列有关镉的说法错误的是( )
 镉是一种重金属元素,在冶金、塑料、电子等行业非常重要.它通常通过废水排入环境中,再通过灌溉进入食物,水稻是典型的“受害作物”,食用后对人体有害.如图,下列有关镉的说法错误的是( )
镉是一种重金属元素,在冶金、塑料、电子等行业非常重要.它通常通过废水排入环境中,再通过灌溉进入食物,水稻是典型的“受害作物”,食用后对人体有害.如图,下列有关镉的说法错误的是( )| A. | 镉的原子序数是 48 | B. | 镉属于非金属元素 | ||
| C. | 镉的元素符号是 Cd | D. | 镉的相对原子质量是 112.4 |
6.归纳与反思是学习化学的重要环节,下列各项归纳完全正确的一组是( )
| A、用“化学”眼光分析 | B、资源的利用和保护 |
| ①洗涤剂去油污是因为起乳化作用 ②气体受压体积缩小是因为气体分子的间隔变小 ③明矾净水是因为明矾溶于水生成胶状物 | ①爱护水资源要节约用水和防止水体污染 ②保护金属资源只能通过防止金属腐蚀实现 ③保护空气要减少有害气体和烟尘的排放 |
| C、物质的分类 | D、“低碳经济”的措施 |
| ①合成橡胶、塑料、合金都属于合成材料 ②由不同种元素组成的物质一定是化合物 ③纯碱、火碱、熟石灰都属于碱 | ①改造或淘汰高能耗、高污染企业 ②研制和开发新能源替代传统能源 ③提倡使用一次性塑料方便袋 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
3.下列说法正确的是( )
| A. | CO 可使澄清石灰水变浑浊 | |
| B. | 铁制品在潮汉空气中比在干燥空气中更易腐蚀 | |
| C. | 合金中只有金属元素 | |
| D. | 金刚石和石墨的硬度都很大 |