题目内容
1.某学习小组在做氢气还原氧化铜的实验时,在试管内加入氧化铜固体10g,通入氢气一会儿后再给氧化铜加热,反应完全后撤去酒精灯并停止通入氢气,在空气中将试管冷却,发现部分红色团体又变回黑色,称得试管中剩余固体质量为8.32克.(1)“在空气中将反应装置冷却”,由红色固体转变成的黑色物质中,氧元素的百分含量为多少?
(2)按此实验操作及获得的数据,可知试管剩余固体中有多少克氧化铜?
分析 加热条件下,氧化铜和氢气反应生成铜和水;
加热条件下,铜和氧气反应生成氧化铜,根据提供的数据可以进行相关方面的计算和判断.
解答 解:(1)10g氧化铜中铜元素的质量为:10g×$\frac{64}{80}$×100%=8g,
由红色固体转变成的黑色物质是氧化铜,氧化铜中氧元素的百分含量为:$\frac{16}{80}$×100%=20%,
答:由红色固体转变成的黑色物质是氧化铜,氧化铜中氧元素的百分含量为20%.
(2)8.32g固体中铜元素的质量是8g,氧元素质量为:8.32g-8g=0.32g,
试管剩余固体中氧化铜质量为:0.32g÷20%=1.6g,
答:试管剩余固体中氧化铜质量为1.6g.
点评 本题是借助于数学模型,利用公式来分析和解决化学计算中的有关问题,要求学生有较强的数据分析能力.

练习册系列答案
相关题目
11.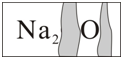 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠(或NaCl)溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠的原子个数为1,而标签中为2.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(3)该瓶无色溶液的溶质是碳酸钠(或Na2CO3).生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
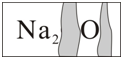 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠(或NaCl)溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠的原子个数为1,而标签中为2.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实 验 操 作 | 实 验 现 象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液. ②静置后,倾去上层清液,向沉淀中滴加稀盐酸. | 产生白色沉淀. 产生大量气泡,沉淀消失. |
(3)该瓶无色溶液的溶质是碳酸钠(或Na2CO3).生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实 验 操 作 | 实 验 现 象 |
| 取少量无色溶液于试管中,向其中滴加稀盐酸 | 有大量气泡产生 |
12.某实验小组取用生石灰时,发现装满生石灰的塑料试剂瓶已经膨胀破裂,小军认为生石灰已变质,试剂瓶中可能含有CaO、Ca(OH)2、CaCO3等三种物质,并开展如下探究:
请回答:
(1)原试剂瓶中可能含有CaCO3的原因是Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示);
(2)小明认为甲方案不够合理,理由是氢氧化钙属于微溶于水的,也会产生白色沉淀,氧化钙与水反应生成氢氧化钙,也会出现白色浑浊;
(3)小红认为放置时间过长,可能全部变成了CaCO3,请你利用实验验证小红的猜想加入盐酸,有气泡放出,再向溶液中加入无色酚酞试液,如果酚酞不变色,说明全部变成了碳酸钙;
(4)小林认为不可能全部变成CaCO3,一定还有CaO,请你设计实验验证小林的猜想将生石灰样品放入试管内,加入水,用手摸试管外壁如果发烫,说明有氧化钙.
| 实验操作 | 实验现象 | 结论 | |
| 甲 | 取试样加入水中,充分搅拌 | 产生白色浑浊 | 一定含有CaCO3 |
| 乙 | 取试样加入稀盐酸中 | 产生无色气泡 | 一定含有CaCO3 |
(1)原试剂瓶中可能含有CaCO3的原因是Ca(OH)2+CO2═CaCO3↓+H2O(用化学方程式表示);
(2)小明认为甲方案不够合理,理由是氢氧化钙属于微溶于水的,也会产生白色沉淀,氧化钙与水反应生成氢氧化钙,也会出现白色浑浊;
(3)小红认为放置时间过长,可能全部变成了CaCO3,请你利用实验验证小红的猜想加入盐酸,有气泡放出,再向溶液中加入无色酚酞试液,如果酚酞不变色,说明全部变成了碳酸钙;
(4)小林认为不可能全部变成CaCO3,一定还有CaO,请你设计实验验证小林的猜想将生石灰样品放入试管内,加入水,用手摸试管外壁如果发烫,说明有氧化钙.
9.2月29日,新发布的《环境空气质量标准》中增加了PM2.5监测指标.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,对人体健康影响更大,主要来源之一是化石燃料的燃烧.下列措施能减少PM2.5污染的是( )
| A. | 鼓励开私家车出行 | B. | 鼓励使用太阳能热水器 | ||
| C. | 鼓励用煤火力发电 | D. | 鼓励用液化石油气作燃料 |
5.判断蜡烛燃烧是化学变化的依据是( )
| A. | 发出黄白色火焰 | B. | 固态石蜡变成了液态 | ||
| C. | 生成了二氧化碳和水 | D. | 放出了大量的热 |
2.2015年12月10日,我国科学家屠呦呦因她“发现青蒿素”(化学式为C15H22O5)成为第一位获得诺贝尔生理医学奖的本土中国科学家!下列关于青蒿素的说法不正确的是( )


| A. | 青蒿素中含有碳、氢、氧三种元素 | |
| B. | 一个青蒿素分子中含有42个原子 | |
| C. | 青蒿素的相对分子质量为282g | |
| D. | 青蒿素中C、H、O三种元素的质量比为90:11:40 |
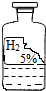 某初级中学学生发现实验室里有一瓶标签破损的无色溶液(如图所示),于是在老师的指导下进行如下探究.
某初级中学学生发现实验室里有一瓶标签破损的无色溶液(如图所示),于是在老师的指导下进行如下探究.