题目内容
工业上用高温煅烧石灰石(主要成分为CaCO3)来制取二氧化碳.现有100吨石灰石样品经高温煅烧一段时间,冷却后称量残留固体质量为78吨,则:
(1)100吨-78吨=22吨表示为______的质量;
(2)计算已分解的碳酸钙的质量(要求写出解题过程).
解:(1)由质量守恒定律可知固体减少的质量即为生成的二氧化碳质量;
(2)设发生分解的碳酸钙的质量为x.
CaCO3 CaO+CO2↑
CaO+CO2↑
100 44
x 22t
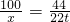
x=50t
故答案为:(1)二氧化碳;(2)答:已分解的碳酸钙的质量是50吨;
分析:由质量守恒定律可知固体减少的质量为二氧化碳的质量,由二氧化碳的质量根据碳酸钙分解的化学方程式可以计算出发生分解的碳酸钙的质量.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的关键.
(2)设发生分解的碳酸钙的质量为x.
CaCO3
 CaO+CO2↑
CaO+CO2↑100 44
x 22t
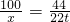
x=50t
故答案为:(1)二氧化碳;(2)答:已分解的碳酸钙的质量是50吨;
分析:由质量守恒定律可知固体减少的质量为二氧化碳的质量,由二氧化碳的质量根据碳酸钙分解的化学方程式可以计算出发生分解的碳酸钙的质量.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列化学方程式书写正确的是
| A.工业上通过高温煅烧石灰石来生产生石灰:CaCO3 ="===" CaO+CO2↑ |
| B.工业上用稀盐酸除铁锈 Fe2O3+ 6HCl="===" 2FeCl2 + 3H2O |
| C.用澄清石灰水检验二氧化碳气体Ca(OH)2+CO2====CaCO3↓+H2O |
| D.用熟石灰处理硫酸厂中的废水Ca(OH)2+H2SO4====CaSO4 +H2O |