题目内容
15.一种元素与另一种元素的本质区别为( )| A. | 电子数 | B. | 中子数 | C. | 质子数 | D. | 以上说法都正确 |
分析 利用元素的定义具有相同的核电荷数(即核内质子数)同一类原子的总称的知识解决此题.
解答 解:元素是具有相同核电荷数(即核内质子数)的一类原子的总称,决定元素种类的是核电荷数(即核内质子数);故不同种元素之间的本质区别是质子数不同.
故选C.
点评 本题难度不大,考查学生对元素的概念的理解和不同种元素之间的本质区别是质子数不同进行解题的能力.

练习册系列答案
 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
5.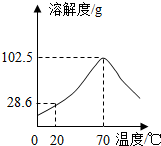 R物质的溶解度曲线如图所示,下列说法正确的是( )
R物质的溶解度曲线如图所示,下列说法正确的是( )
 R物质的溶解度曲线如图所示,下列说法正确的是( )
R物质的溶解度曲线如图所示,下列说法正确的是( )| A. | R的溶解度随温度的升高而增大 | |
| B. | 20℃时,100 gR的饱和溶液中溶质质量为28.6 g | |
| C. | 将70℃时R的饱和溶液升高温度,有晶体析出 | |
| D. | t℃时配制了质量分数为50%的R溶液,则t一定小于70 |
3.近代化学工业是从无机化学产品的生产起步的,特别是“三酸两碱”--硫酸、盐酸、硝酸、纯碱、烧碱.下列关于“三酸两碱”说法错误的是( )
| A. | 纯碱溶液pH>7 | B. | 浓硫酸、浓盐酸可作干燥剂 | ||
| C. | 盐酸可用于除锈 | D. | 硝酸能与烧碱发生中和反应 |
7.某样品为Cu和CuO的混合物,为测定样品中CuO的含量,甲、乙、丙、丁四位学生用同一种样品分别进行实验,测得的数据如表:
分析实验数据,回答下列问题:
(1)写出氧化铜与硫酸反应的化学方程式.
(2)求混合物中氧化铜的质量分数.
(3)求硫酸溶液中溶质的质量分数.
| 学生 物质质量 | 甲 | 乙 | 丙 | 丁 |
| 所取固体样品的质量(g) | 30 | 25 | 20 | 20 |
| 加入硫酸溶液的质量(g) | 100 | 100 | 100 | 120 |
| 反应后剩余固体的质量(g) | 22 | 17 | 12 | 12 |
(1)写出氧化铜与硫酸反应的化学方程式.
(2)求混合物中氧化铜的质量分数.
(3)求硫酸溶液中溶质的质量分数.
5.某科学兴趣小组在课外活动中,对某无色透明溶液进行了多次检测,其中三次检测结果如表所示,请回答:
(1)三次检测结果中第二次检测结果不正确.
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,先向溶液中加入过量的稀HNO3溶液;然后继续加入过量的Ba(NO3)2溶液;过滤后,再向滤液中加入AgNO3溶液.
(3)测得某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子,其中离子个数比为Na+:Mg2+:Cl-=4:5:8.若设Na+为4n个,则SO42-的离子数为3n.
| 检测次数 | 溶液中检测出的物质 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,先向溶液中加入过量的稀HNO3溶液;然后继续加入过量的Ba(NO3)2溶液;过滤后,再向滤液中加入AgNO3溶液.
(3)测得某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子,其中离子个数比为Na+:Mg2+:Cl-=4:5:8.若设Na+为4n个,则SO42-的离子数为3n.