题目内容
3.电解水与分解过氧化氢都可产生氧气,要制取相同质量的氧气,水与过氧化氢的质量比是( )| A. | 9:17 | B. | 1:1 | C. | 17:9 | D. | 无法确定 |
分析 根据过氧化氢的质量可以计算生成氧气的质量,根据氧气的质量可以计算电解水的质量.
解答 解:由2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ 可知,2H2O2~O2~2H2O
即:H2O2~H2O
34 18
产生等质量的氧气需要水与过氧化氢的质量比为:18:34=9:17.
故选A.
点评 本题主要考查学生运关系式法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
13.下列有关氧气化学性质的描述中.不正确的是( )
| A. | 氧气的化学性质比较活泼 | B. | 氧气能供给呼吸 | ||
| C. | 氧气能燃烧 | D. | 氧气具有氧化性 |
11.从下列试验现象推断,黑色粉末可能是( )
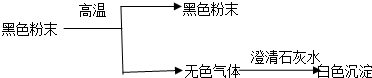

| A. | Fe和CuO | B. | C和CuO | C. | C和Fe3O4 | D. | MnO2和CuO |
18.下列各项不随水质量的变化而变化的是( )
| A. | 溶液中溶质的质量分数 | |
| B. | 物质的溶解度 | |
| C. | 过量的氧化钠与水反应生成的氢氧化钠 | |
| D. | 酸溶液的pH |
13.能反映水的化学性质的变化是( )
| A. | 水蒸发 | B. | 水沸腾 | C. | 水电解 | D. | 水结冰 |
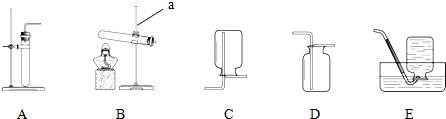
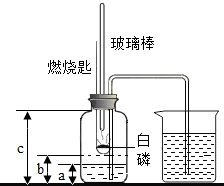 某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置,实验步骤如下:
某校化学研究性学习小组在学习了“空气中氧气含量测定”的基础上,改进了教材中的实验,设计出了如图所示的实验装置,实验步骤如下: 按图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题:
按图组装仪器,关闭止水夹,通电使红磷燃烧.请回答下列问题: