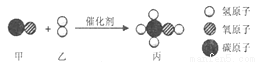
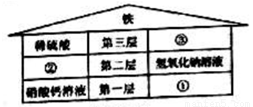
题目内容
碱式氯化镁【Mg(OH)Cl】受热能分解,它分解后产物是什么?小科进行了探究。
【猜想】Mg(OH)Cl分解后产物可能有:Mg、MgCl2、MgO、HCl气体、H2O、Cl2。
老师告诉他产物就是上述猪想中的其中几种,并提示Cl2是一种黄绿色有刺激性气味的气体。
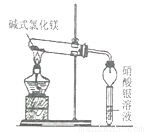
【实验一】取少量的Mg(OH)Cl放入大试管中,按如图所示装置进行实验。加热过程中观察到足量硝酸银溶液中有白色沉淀产生,一段时间后,沉淀不再产生,大试管口也没有液滴形成,管内有固体剩余,无其他现象。由此推知Mg(OH)Cl分解后产物中有_______气体,无其他气体。
【实验二】取少量实验一的剩刹余固体于试管中,加入足量稀盐酸,没有气泡产生。由此推知Mg(OH)Cl分解后产物中没有_______。
【实验三】再取少量实验一的剩余固体,加入足量稀硝酸,固体全部溶解,再滴入AgNO3溶液,无沉淀产生。由此推知Mg(OH)Cl分解后产物中没有________。
【结论】Mg(OH)Cl受热分解的化学反应方程式为____________。
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案小金利用图示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略)。

(1)从实验安全角度考虑,图示装置还应采取的改进措施是_____________。
(2)完全反应后,两组的生成物均为黑色粉末(纯净物),分别用两组生成物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 称量黑色粉末质量/g | m1 | m2 |
2 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
3 | 取黑色粉末,加入稀盐酸 | 全部溶解,有大量气泡 | 无明显现象 |
4 | 取黑色粉末,加入足量CuSO4溶液 | 有红色物质生产 | 无明显现象 |
①甲组的黑色粉末与稀盐酸反应的化学方程式是__________。
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4。他又发现m2恰好为_______g ,这可成为支持上述猜想的新证据。
(3)甲、乙两组实验说明温度对CO和Fe2O3反应有影响,且均体现出CO的__________(填写化学性质)。
小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:
组别 | A | B | C |
试管中依次 加入物质 | 1ml唾液 | 1ml唾液 | 1ml唾液 |
1ml盐酸溶液 | 1ml蒸馏水 | 1ml氢氧化钠溶液 | |
2ml淀粉溶液 | 2ml淀粉溶液 | 2ml淀粉溶液 | |
水浴10分钟 | 37℃ | 37℃ | 37℃ |
各滴入2滴 碘液后的现象 | 变蓝 | 不变蓝 | 不变蓝 |
(1)B组实验不变蓝的原因是____________________。小柯观察到C组也不变蓝,认为氢氧化钠对酶的活性没有影响。老师提示他:“氢氧化钠会影响酶的活性。”那么,是什么原因导致C组没变蓝?小柯进一步分析并做出猜想。
猜想一:氢氧化钠变质。
猜想二:氢氧化钠与碘发生了化学反应。
……
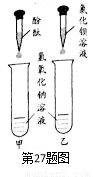
(2)小柯按图甲实验,看到溶液变红,认为氢氧化钠没有变质。小常认为他的结论是
错误的,理由是_________________________。
在小常的建议下,小柯按乙实验,溶液中没有沉淀产生,从而排除了猜想一。
(3)在原来C组实验基础上,只要继续_______________________(写出操作和现象),就可以证明猜想二正确。