题目内容
20.现有表面被氧化的镁条样品11.2g,加入到盛有400g7.3%的稀盐酸的烧杯中,恰好完全反应.则被氧化的镁占原镁条的质量分数为( )| A. | 75% | B. | 25% | C. | 85% | D. | 33% |
分析 氧化镁和盐酸生成氯化镁和水;镁和盐酸生成氯化镁和氢气.写出化学方程式可以计算出氧化镁的质量;然后根据氧化镁的质量计算出变成氧化镁的镁的质量,最后计算出被氧化的镁占原镁条的质量分数.
解答 解:设氧化镁的质量是x,氧化镁消耗盐酸的质量为y;镁的质量为11.2g-x,消耗盐酸的质量为z
MgO+2HCl═MgCl2+H2O
40 73
x y
$\frac{40}{73}=\frac{x}{y}$
y=$\frac{73x}{40}$
Mg+2HCl═MgCl2+H2↑
24 73
11.2g-x z
$\frac{24}{73}=\frac{11.2g-x}{z}$
z=$\frac{73×(11.2g-x)}{24}$
y+z=400g×7.3%
x=4g
设生成4克氧化镁需要镁的质量是w
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO
48 80
w 4g
$\frac{48}{80}=\frac{w}{4g}$
w=2.4g
被氧化的镁占原镁条的质量分数为:$\frac{2.4g}{2.4g+11.2g-4g}$×100%=25%
故选:B.
点评 本题主要考查了化学方程式的计算,难度适中,注意解题的规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.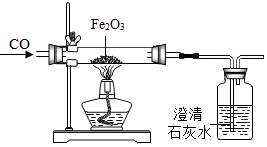 如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )
如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )
 如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )
如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )| A. | 该装置缺少尾气处理装置,会污染空气 | |
| B. | 点燃酒精灯前应持续通入CO防止发生爆炸 | |
| C. | 改用二氧化碳进行该实验也能看到完全相同的现象 | |
| D. | 利用反应前后固体质量之差能算出参加反应的一氧化碳的质量 |
11.下列有关化学方程式2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO含义的叙述中,正确的是( )
| A. | 该反应的生成物是氧化铜 | |
| B. | 该反应条件是加热 | |
| C. | 该反应中,铜和氧气的质量比为2:1 | |
| D. | 该反应中,Cu、O2、CuO的微粒个数比为2:1:2 |
1.下列关于资源、能源的叙述正确的是( )
| A. | 使化石燃料充分燃烧,既可以减少空气污染.又可以节约化石能源 | |
| B. | 空气的成分按体积计大约是:氮气和氧气占99%,稀有气体占1% | |
| C. | 海洋蕴藏着丰富的化学资源,目前测定海水中含有的物质有80多种 | |
| D. | 人类可直接利用的淡水资源占全球总储水量的2.53% |
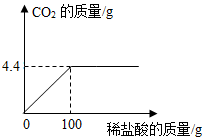 某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答:
某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答: