题目内容
16.有一不纯的硝酸铵化肥样品(主要成分是NH4NO3)经分析知道其中氮的质量分数为38%则该化肥可能混入了( )| A. | NH4Cl(含氮约26%) | B. | (NH4)2SO4(含氮约21%) | ||
| C. | NH4HCO3(含氮约17.7%) | D. | CO(NH2)2(含氮约46.7%) |
分析 先求出硝酸铵中氮元素的质量分数,然后与38%比较,再利用平均值法则解决并判断选项即可.
解答 解:NH4NO3氮元素的质量分数为 $\frac{2×14}{2×14+4+16×3}$×100%=35%,小于38%,故混入的化肥含氮量大于38%
故选D.
点评 此题是结合平均值法则进行的化学式计算考查题,是对学生进行的常规计算及方法的训练.

练习册系列答案
 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
11.下列关于玻璃仪器洗涤的描述,错误的是( )
| A. | 玻璃仪器的洗涤通常配合使用试管刷进行 | |
| B. | 滴瓶上的滴管用后洗涤干净再放回原瓶 | |
| C. | 清洗完毕试管应该倒插在试管架上 | |
| D. | 玻璃仪器洗干净的标志是既不聚成水滴,也不成股流下 |
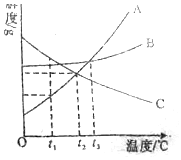 如图A、B、C为三种物质的溶解度曲线,据图回答.
如图A、B、C为三种物质的溶解度曲线,据图回答.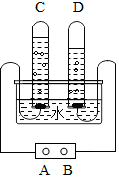 如图是电解水的简易装置.回答下列各问题:
如图是电解水的简易装置.回答下列各问题: