题目内容
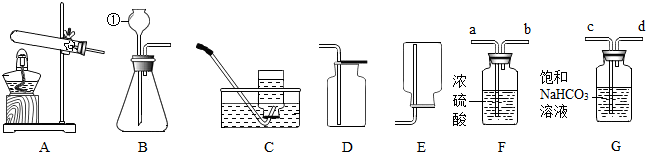
2.根据如图回答问题.
(1)图1锥形瓶中充满二氧化碳,将分液漏斗中滴有紫色石蕊的溶液加入到瓶中,观察到气球胀大现象证明二氧化碳与水反应.
(2)图2配制一定质量10%的稀硫酸,图2操作中用玻璃棒搅拌的目的是散热.
(3)图3玻璃管中发生反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,铁架台是由铁合金制成的,铁架台的防锈措施是刷漆(写一点即可).
分析 (1)若关闭弹簧夹,把注射器中的氢氧化钠溶液加入到锥形瓶中,瓶内二氧化碳与氢氧化钠溶液反应,使瓶内气体减少,压强变小,小于外界大气压,在大气压的作用下,气球胀大;
(2)根据浓硫酸的稀释方法进行分析玻璃棒的作用解答;
(3)根据一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,以及铁生锈的原理进行分析.
解答 解:(1)若关闭弹簧夹,把注射器中的氢氧化钠溶液加入到锥形瓶中,观察到的现象有:气球变大;产生此现象的原因是:二氧化碳与氢氧化钠溶液反应,使瓶内气体减少,压强变小,小于外界大气压,在大气压的作用下,气球变大;
(2)稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时地扩散;一定不能把水注入浓硫酸中;
(3)一氧化碳和氧化铁在高温的条件下生成铁和二氧化碳,化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,铁架台是由铁合金制成的,铁架台的防锈措施是刷漆.
故答案为:(1)气球变大;
(2)散热;
(3)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,刷漆.
点评 本题难度不大,考查了氢氧化钠的性质、浓硫酸的稀释和铁的冶炼,掌握浓硫酸的稀释方法、溶质质量分数的有关计算并能灵活运用是正确解答本题的关键.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案
相关题目
13.下列各项中不属于化学反应的是( )
| A. | 用活性炭除去冰箱中的异味 | B. | 用胃舒平治疗胃酸过多 | ||
| C. | 在蔗糖中加入浓硫酸后变黑 | D. | 煤的干馏和食品的腐败 |
7.如图所示的实验操作不正确的是( )
| A. |  铁丝在氧气中燃烧 | B. |  读取液体的体积 | ||
| C. | 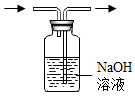 除去CO中的CO2 | D. |  加热液体 |
14.下列知识归纳中,完全正确的一组是( )
| A、化学知识 | B、化学与健康 |
| ①活性炭除异味是利用它的吸附性 ②合金、塑料、橡胶都属于合成材料 | ③人体缺乏维生素C易患坏血病 ④海鲜防腐可用甲醛溶液浸泡 |
| C、化学与生活 | D、化学与环境 |
| ⑤用汽油清洗油污属于乳化作用 ⑥用燃烧法区分棉纤维和羊毛纤维 | ⑦使用无磷洗衣粉可减少水污染 ⑧使用可降解塑料可减少“白色污染” |
| A. | A | B. | B | C. | C | D. | D |