题目内容
13.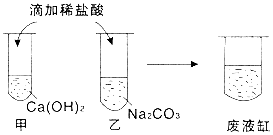 甲、乙同学在学完酸的化学性质后,做了如下实验:
甲、乙同学在学完酸的化学性质后,做了如下实验:实验结束,甲、乙同学依次将废液倒入同一洁净的废液缸中,观察到废液缸中先有少量气泡产生,最终有白色沉淀生成.回答:
(1)废液缸中生成的白色沉淀是碳酸钙.
(2)乙实验后的废液中含有的溶质是氯化氢、氯化钠.
(3)将废液缸中的废液取出过滤,所得滤液中一定含有的溶质是氯化钠.
(4)若所得滤液中还含有CaCl2,请你设计简单的方案证明之(写出实验步骤和实验现象)取样品,加入足量的碳酸钠,有白色沉淀生成,说明含有氯化钙.
分析 根据实验结束,甲、乙同学依次将废液倒入同一洁净的废液缸中,先有气泡产生,然后又出现了白色沉淀,说明液体中有酸、碳酸根及钙离子,所以知甲同学的试管:CaCl2、HCl,乙试管中含有碳酸钠、氯化钠,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠进行分析.
解答 解:实验结束,甲、乙同学依次将废液倒入同一洁净的废液缸中,先有气泡产生,然后又出现了白色沉淀,说明液体中有酸、碳酸根及钙离子,所以知甲同学的试管:CaCl2、HCl,乙试管中含有碳酸钠、氯化钠,氯化钙和碳酸钠反应生成碳酸钙沉淀和氯化钠,所以
(1)废液缸中生成的白色沉淀是碳酸钠和氯化钙反应生成的碳酸钙沉淀;
(2)通过推导可知,乙实验后的废液中含有的溶质是:氯化氢、氯化钠;
(3)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,所以将废液缸中的废液取出过滤,所得滤液中一定含有的溶质是氯化钠;
(4)若所得滤液中还含有CaCl2,设计简单的方案是:取样品,加入足量的碳酸钠,有白色沉淀生成,说明含有氯化钙.
故答案为:(1)碳酸钙沉淀;
(2)氯化氢、氯化钠;
(3)氯化钠;
(4)取样品,加入足量的碳酸钠,有白色沉淀生成,说明含有氯化钙.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
3.2017年6月5日“世界环境日”中国主题是“绿水青山就是金山银山”.下列做法不符合这一主题的是
( )
( )
| A. | 工业废水处理后再排放 | B. | 使用共享自行车代替汽车出行 | ||
| C. | 开发利用各种清洁能源 | D. | 大量使用农药提高家作物产量 |
1.下列图示的实验操作正确的是( )
| A. | 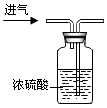 干燥氧气 | B. | 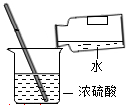 稀释浓硫酸 | C. |  测定溶液的pH | D. | 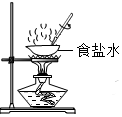 蒸发食盐水 |
8.如图为实验室制取气体的常见装置:
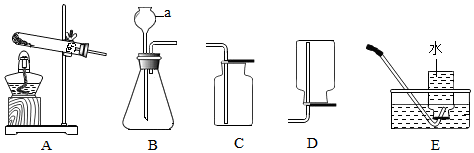
(1)仪器a的名称是长颈漏斗;
(2)以A为发生装置,用高锰酸钾制取氧气,化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取并收集二氧化碳,选择的装置组合是BC(填标号);
(4)温度、浓度、固体的颗粒大小等因素会影响反应速率,为研究实验室制取二氧化碳的适宜条件,进行如表四组实验:
①大理石与盐酸反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑;
②实验甲与丙对照(填标号),是为了研究固体反应物颗粒大小对反应速率的影响;
③上述实验中,另一个影响反应速率的因素是反应物的浓度.

(1)仪器a的名称是长颈漏斗;
(2)以A为发生装置,用高锰酸钾制取氧气,化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)实验室制取并收集二氧化碳,选择的装置组合是BC(填标号);
(4)温度、浓度、固体的颗粒大小等因素会影响反应速率,为研究实验室制取二氧化碳的适宜条件,进行如表四组实验:
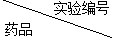 | 甲 | 乙 | 丙 | 丁 |
| ag大理石 | 块状 | 块状 | 粉末状 | 粉末状 |
| bg盐酸(过量) | 稀盐酸 | 浓盐酸 | 稀盐酸 | 浓盐酸 |
②实验甲与丙对照(填标号),是为了研究固体反应物颗粒大小对反应速率的影响;
③上述实验中,另一个影响反应速率的因素是反应物的浓度.
18.日常生活中除去油污的方法很多,下列现象不属于乳化的是( )
| A. | 用汽油洗去手上的油污 | B. | 用香皂洗去身上的油脂 | ||
| C. | 洁面乳洗去皮肤上的油脂 | D. | 洗洁精洗去餐具上的油污 |
3.下列关于原子的叙述正确的是( )
| A. | 原子都是由质子、中子和核外电子构成的 | |
| B. | 整个原子的质量主要集中在原子核外的较大空间 | |
| C. | 原子通过得失电子可以变成其他元素的离子 | |
| D. | 原子中质子与电子所带电荷的数量相等,电性相反,所以原子不显电性 |
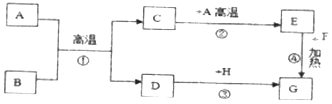
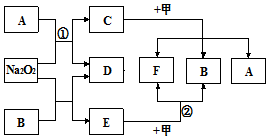 过氧化钠(化学式:Na2O2)常用作供氧剂.图中,A~F是初中阶段常见的化学物质.常温下,A、D是气体,F是日常生活中调味品的主要成分.
过氧化钠(化学式:Na2O2)常用作供氧剂.图中,A~F是初中阶段常见的化学物质.常温下,A、D是气体,F是日常生活中调味品的主要成分.