题目内容
8.某校学生要进行一系列实验,请结合下图帮助他们解决以下问题: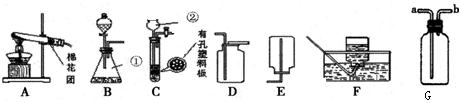
(1)写出编号所指仪器的名称:①锥形瓶;②长颈漏斗.
(2)向气体发生装置内加入药品前,应该进行的操作是检验装置的气密性.
(3)实验室利用A装置制取氧气,试管口放棉花的作用是防止高锰酸钾飞溅堵塞导管,反应原理用化学方程式表示为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;,基本反应类型是分解反应,收集装置选择D或F.
(4)实验室用C装置制取二氧化碳,使用该装置制取气体的突出优点是控制反应速率,反应原理用化学方程式表示为CaCO3+2HCl=CaCl2+CO2↑+H2O,收集装置是D(填序号),验满的方法是用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳.
(5)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,你认为用G图收集氨气应从b(填a或b)端通入,理由是氨气的密度比空气小.
分析 (1)据常用仪器回答;
(2)向气体发生装置内加入药品前,要检验装置的气密性;
(3)据A装置是加热固体制取氧气,且试管口有棉花可知是用加热高锰酸钾的方法制取氧气,并据反应原理书写方程式,据反应特点和注意事项解答;
(4)据实验室制取二氧化碳的反应原理书写方程式,据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,分解反应的特点是‘一变多’二氧化碳验满的方法是用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;
(5)据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置.
解答 解:(1)装置中标出的仪器名称①锥形瓶、②长颈漏斗;
(2)向气体发生装置内加入药品前,要检验装置的气密性;
(3)A装置是加热固体制取氧气,且试管口有棉花可知是用加热高锰酸钾的方法制取氧气,加热时在试管口放棉花是为了防止加热时高锰酸钾粉末进入导管反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应由一种物质生成三种物质,属于分解反应,因氧气密度比空气大,不易溶于水,故可用向上排空气法或排水法收集;
(4)实验室用C装置制取二氧化碳,使用该装置制取气体的突出优点是可控制反应速率;实验室用大理石和稀盐酸制取二氧化碳,反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;因为二氧化碳的密度比空气大,能溶于水,可以用向上排气法收集,验满的方法是用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;
(5)实验室用加热氯化铵和氢氧化钙固体混合物的方法制取氨气,若用如G图所示装置收集氨气,由于氨气的密度比空气小,氨气应从导管b通入.
故答案为:(1)锥形瓶、长颈漏斗;(2)检验装置的气密性;
(3)防止高锰酸钾飞溅堵塞导管、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;分解反应;D或F;
(4)可控制反应速率、CaCO3+2HCl═CaCl2+H2O+CO2↑;D;用燃着的木条放在瓶口,如果木条熄灭则说明瓶内已收集满二氧化碳;
(5)b、氨气的密度比空气小.
点评 本题主要考查了化学方程式的书写、实验装置的选择及其判断仪器的名称等方面的知识.完成此题,可以依据已有的知识进行.

 应用题作业本系列答案
应用题作业本系列答案| A. | 锌粒与盐酸反应比铁片与盐酸反应要剧烈,故锌比铁活泼 | |
| B. | 中和反应一定生成盐和水,但生成盐和水的反应不一定是中和反应 | |
| C. | 燃烧一般都伴随发光和放热现象,所以有发光和放热现象的变化都是燃烧 | |
| D. | 原子不显电性,所以构成原子的粒子也不显电性 |
| A. | N${\;}_{5}^{+}$是一种新的原子 | |
| B. | N${\;}_{5}^{+}$是由五个氮原子构成的分子 | |
| C. | N${\;}_{5}^{+}$是带一个单位正电荷的阳离子 | |
| D. | N${\;}_{5}^{+}$是带一个单位负电荷的阴离子 |
 )与B(
)与B(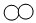 )反应生成C(
)反应生成C(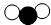 )及反应前后分子及其数目的变化,则该反应的化学方程式中,化学计量数之比为( )
)及反应前后分子及其数目的变化,则该反应的化学方程式中,化学计量数之比为( )
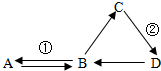 已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如右图所示(部分物质和反应条件已略去).
已知:反应①是实验室制取气体A的常用方法,D常用来改良酸性土壤,它们之间的转化关系如右图所示(部分物质和反应条件已略去). 人体中钙元素主要以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]形式存在于骨骼和牙齿中,牛奶是含钙丰富又易吸收的理想食品,根据如图某乳业公司纯牛奶包装标签:
人体中钙元素主要以羟基磷酸钙晶体[Ca10(PO4)6(OH)2]形式存在于骨骼和牙齿中,牛奶是含钙丰富又易吸收的理想食品,根据如图某乳业公司纯牛奶包装标签: