题目内容
15.我市某冶炼厂购进了100t“铜灰”(主要成分是CuO和不参与反应的杂质),某兴趣小组同学在这批铜灰中进行取样,并称取样品5g,进行如图所示实验,直到反应完全.冷却后对玻璃管内的残留固体进行称量,其质量为4.2g,此时,石灰水的质量增加了1.76g,对于实验测得的数据怎样用于计算,组内同学有不同的意见:(提示:反应为CO+CuO $\frac{\underline{\;高温\;}}{\;}$Cu+CO2,实际反应中石灰水不能完全吸收二氧化碳.)
(1)小许认为要用“4.2g”这个数据,请你用这个数据计算5g铜灰还原后能生成几克铜?
(2)小黄认为要用“1.76g”这个数据,请你帮小黄计算5g铜灰还原后能生成几克铜?
(3)试比较小许和小黄谁错了?为什么?计算100t铜灰最多可冶炼出多少吨纯净的铜?
分析 氧化铜和一氧化碳在高温条件下反应生成铜和二氧化碳,反应前后的质量差即为氧化铜中铜元素的质量,根据反应的化学方程式和提供的数据可以进行相关方面的计算和判断.
解答 解(1)设生成铜的质量为x,
反应前后的质量差即为氧化铜中氧元素的质量,
CuO~O~Cu,
16 64
5g-4.2g x
$\frac{16}{5g-4.2g}$=$\frac{64}{x}$,
x=3.2g,
答:5g铜灰还原后生成铜的质量为3.2g.
(2)设生成铜的质量为y,
CuO+CO$\frac{\underline{\;高温\;}}{\;}$Cu+CO2,
64 44
y 1.76g
$\frac{64}{y}$=$\frac{44}{1.76g}$,
y═2.56g,
答:5g铜灰还原后生成铜的质量为2.56g.
(3)小黄错了,这是因为实际反应中石灰水不能完全吸收二氧化碳,会导致计算结果偏小.
设生成铜的质量为z,
由(1)中可知,5g铜灰完全反应能够生成3.2g铜,
铜灰~Cu,
5g 3.2g
100t z
$\frac{5g}{100t}$=$\frac{3.2g}{z}$,
z=64t,
答:生成铜的质量为64t.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 期末金牌卷系列答案
期末金牌卷系列答案 轻松课堂标准练系列答案
轻松课堂标准练系列答案
相关题目
5.学习了MnO2对过氧化氢分解有催化作用的知识后.某同学想:CuO能否起到类似MnO2的催化作用呢?于是进行了以下探究.
[猜想]Ⅰ、CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;‘
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后质量和化学性质不变
【实验】
用天平称量0.2g CuO,取5ml5%过氧化氢溶液于试管中,进行实验: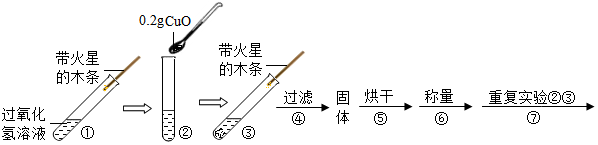
(1)完成如表
(2)步骤①的目的和②、③对比
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为:过氧化氢$\stackrel{氧化铜}{→}$水+氧气
【拓展】由上述实验可知,作为催化剂的三点条件为:能够改变化学反应的速率、反应前后质量不变、反应前后化学性质不变.
[猜想]Ⅰ、CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;‘
Ⅱ、CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后质量和化学性质不变
【实验】
用天平称量0.2g CuO,取5ml5%过氧化氢溶液于试管中,进行实验:

(1)完成如表
| 步骤的现象 | 步骤⑥的结果 | 步骤⑦的现象 | 结论 |
| 带火星的木条复燃 | 0.2g | 溶液中有气泡放出 | 猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(3)过氧化氢能被氧化铜催化分解放出氧气的文字表达式为:过氧化氢$\stackrel{氧化铜}{→}$水+氧气
【拓展】由上述实验可知,作为催化剂的三点条件为:能够改变化学反应的速率、反应前后质量不变、反应前后化学性质不变.
6.新一代功能性健康型饮料苹果醋(ACV)具有提高人体免疫能力、抗衰老、软化血管等作用,其主要成分之一是苹果酸(C4H6O5).下列说法中正确的是( )
| A. | 苹果酸饮料的pH>7 | |
| B. | 苹果酸中碳、氢、氧三种元素的质量比为4:6:5 | |
| C. | 苹果酸不可用铝制容器盛放 | |
| D. | 苹果酸属于纯净物 |
3.下列事实与金属活动性无关的是( )
| A. | 铁桶不能配置波尔多液 | |
| B. | 课本上用锌、铜完成化学能转化成电能的实验 | |
| C. | 稀盐酸除铁锈 | |
| D. | 新铝锅烧过含铁离子的水后锅内会发黑 |
4.有同学的化学笔记上有以下知识总结,你认为不正确的是( )
| A. | 元素是质子数相同的一类原子的总称,因此质子数相同的粒子一定是同种元素的原子 | |
| B. | 分子是由原子构成的,因此分子的质量一定大于原子的质量 | |
| C. | CO有毒而CO2无毒,因此不同种分子化学性质不相同 | |
| D. | 物质分纯净物和混合物,由一种元素组成的物质不一定是单质 |
 用浓盐酸和石灰石反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.为此,同学们进行了探究.
用浓盐酸和石灰石反应,将得到的气体X通入澄清石灰水中,始终没有发现石灰水变浑浊.为此,同学们进行了探究. 如图是某盐场生产并处理过的工业盐产品质量指标.某学生为了测定该工业盐中氯化钠的质量分数,进行如下实验:(1)取100克该工业盐加热烘干,测得水的质量为3.36克;(2)另取100克该工业盐溶于水中加入足量碳酸钠溶液得到碳酸钡沉淀1.97克(反应的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl).
如图是某盐场生产并处理过的工业盐产品质量指标.某学生为了测定该工业盐中氯化钠的质量分数,进行如下实验:(1)取100克该工业盐加热烘干,测得水的质量为3.36克;(2)另取100克该工业盐溶于水中加入足量碳酸钠溶液得到碳酸钡沉淀1.97克(反应的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl).