题目内容
(1)已知一个碳原子质量为1.992×10﹣26kg,一个硫原子的质量为5.315×10﹣26kg,请根据有关知识计算:
①硫原子的相对原子质量(结果保留整数);
②若该硫原子核外电子数为16,则它的中子数是多少?
(2)硫酸钾的相对分子质量是 ,其中钾元素、硫元素、氧元素的质量比为 .
(3)请计算多少克硫酸钾中钾元素质量与14.9克氯化钾中钾元素质量相等?
答案 分析: (1)①根据某原子的相对原子相对质量= ,结合题意进行分析解答即可.
,结合题意进行分析解答即可.
②根据相对原子质量=质子数+中子数;
(2)根据化学式的意义进行分析,相对分子质量是所有原子相对原子质量的总和,元素的质量比等于各原子相对原子质量和之比,根据元素的含量可以确定元素的质量分数,从而求出元素的质量.
(3)根据元素的质量=化合物的质量×元素的质量分数;
解答: 解:(1)①根据某原子的相对原子相对质量= ,硫原子的相对原子质量=
,硫原子的相对原子质量=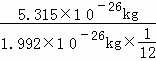 =32;
=32;
②硫原子中子数=32﹣16=16;
答案:32;16;
(2)硫酸钾的相对分子质量为:39×2+32+16×4=174;
硫酸钾中钾元素、硫元素、氧元素的质量比为:39×2:32:16×4=39:16:32;
答案:174;39:16:32;
(3)设质量为x的硫酸钾中钾元素质量与14.9克氯化钾中钾元素质量相等;
x×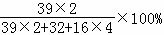 =14.9g×
=14.9g×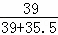
x=17.4g
答:17.4g的硫酸钾中钾元素质量与14.9克氯化钾中钾元素质量相等

练习册系列答案
相关题目
 素组成的
素组成的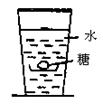 某同学在家做右图所示的实验:在一个玻璃容器中加入100 ml水,向水中放入一块糖,在容器外壁沿液面划一条水平线,过一会儿发现糖块溶解,液面比原来水平面降低了。通过这一现象请你推测分子具有 、 性质。
某同学在家做右图所示的实验:在一个玻璃容器中加入100 ml水,向水中放入一块糖,在容器外壁沿液面划一条水平线,过一会儿发现糖块溶解,液面比原来水平面降低了。通过这一现象请你推测分子具有 、 性质。