题目内容
7.下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |
①加入Ca(OH)2 ②升高温度 ③降低温度 ④加入水 ⑤蒸发水后再恢复到原温度 ⑥加入生石灰.其中正确的是D.
A.②④⑥B.③④C.①③⑤⑥D.①②⑤⑥
(2)20℃时,将191g饱和NaOH溶液蒸发10g水后,再降温到20℃,可析出NaOH晶体的质量为9.1g.
(3)18℃时Ca(OH)2的饱和溶液中,溶质的质量分数为m%.向其中加入一定量的CaO后所得溶液中,溶质的质量分数为n%.则m%>n%(填“>”、“<”或“=”).
(4)现有60℃时含Ca(OH)2和NaOH两种物质的饱和溶液,若要从其中得到较纯净的NaOH晶体,可采取的物理方法是降温结晶.
(5)20℃时,欲测定某NaOH溶液的pH,若先将pH试纸用蒸馏水润湿再进行测定,则所测得溶液的pH偏小(填“偏大”、“偏小”或“不受影响”).
分析 (1)根据CaO和水反应生成氢氧化钙,放出热量,而Ca(OH)2的溶解度随温度的升高而减小,据此解答;
(2)根据20℃时NaOH的溶解度分析回答;
(3)根据CaO和水反应生成氢氧化钙,放出热量,而Ca(OH)2的溶解度随温度的升高而减小,并结合饱和溶液溶质的质量分数计算式分析解答;
(4)根据氢氧化钠的溶解度随温度的降低而减小,氢氧化钙的溶解度随温度的减小而增大进行解答;
(5)根据将pH试纸用蒸馏水润湿,再进行测定氢氧化钠溶液的pH值,会使得氢氧化钠溶液的碱性变弱进行解答.
解答 解:(1)①加入氢氧化钙,能使不饱和溶液变为饱和溶液;②升高温度,氢氧化钙的溶解度减小,可以由不饱和溶液变为饱和溶液;③降低温度,氢氧化钙的溶解度增大,不能变为饱和溶液;④加入水,不能变为饱和溶液;⑤蒸发水后再恢复到原温度,可以由不饱和溶液变为饱和溶液;⑥加入生石灰,则氧化钙和水反应生成氢氧化钙,会使溶液变为饱和溶液,观察选项,故选D;故填:D;
(2)20℃时NaOH的溶解度是91g,则10g水最多溶解9.1g,所以191g 饱和NaOH溶液,蒸发10g水后,再降温到20℃,可析出NaOH晶体9.1g;故填:9.1g;
(3)CaO和水反应生成氢氧化钙,放出热量,而Ca(OH)2的溶解度随温度的升高而减小,饱和溶液溶质的质量分数计算式$\frac{溶解度}{溶解度+100g}$×100%,即溶解度越大质量分数也就越大,所以加入一定量CaO后得到的溶液的溶解度小于原溶液,此时溶液的质量分数关系是m%大于n%;故填:>;
(4)氢氧化钠的溶解度随温度的降低而减小,氢氧化钙的溶解度随温度的减小而增大,现有60℃时含Ca(OH)2和NaOH两种物质的饱和溶液,若要从其中得到较纯净的NaOH晶体,可采取的物理方法是降温结晶;故填:降温结晶;
(5)将pH试纸用蒸馏水润湿,再进行测定氢氧化钠溶液的pH值,会使得氢氧化钠溶液的碱性变弱,所以则所测得溶液的pH偏小.故填:偏小.
点评 了解Ca(OH)2、NaOH溶解度的溶解度随温度的变化情况,测定溶液pH值的正确方法,并能据所学知识正确分析解答,本题重在考查对知识的掌握和应用,培养学生分析解决问题的能力.

 智能训练练测考系列答案
智能训练练测考系列答案| A. | 溶解度为34g | |
| B. | 是一种易溶物 | |
| C. | 溶质质量分数的最大值为30% | |
| D. | 若要使20℃时饱和溶液的质量分数增大一倍,可采用蒸发溶剂的方法 |
| A. | 石油分馏 | |
| B. | 风能发电 | |
| C. | 从铝土矿(主要成分是Al2O3)中提炼金属铝 | |
| D. | 海水晒盐 |
| A. | 食物腐烂 | B. | 冰雪融化 | C. | 玻璃破碎 | D. | 香水扩散 |
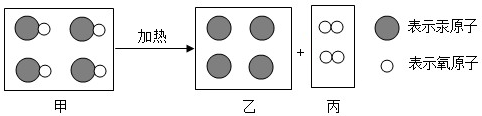
| A. | 图中甲、乙、丙三种物质均是由分子构成的 | |
| B. | 图中甲、乙、丙三种物质中,乙、丙属于单质 | |
| C. | 该反应前后分子种类、原子种类均没有改变 | |
| D. | 该反应是化合反应 |
| A. | 干冰用于人工降雨 | B. | 用氢氧化钠改良酸性土壤 | ||
| C. | 用氢气作燃料 | D. | 用氢氧化铝治疗胃酸过多 |
 化学与健康
化学与健康“APEC”会议的晚宴上有一道传统小吃“豌豆黄”,根据表格中的信息回答下列问题.
| 品名 | 豌豆黄 |
| 主要原料 | 豌豆 |
| 主要营养成分 | 蛋白质、糖类、钠、钙、钾、镁等元素 |
(2)“豌豆黄”中含有钙元素.人体缺钙常会引起BD(填字母序号).
A.贫血症 B.佝偻病 C、甲状腺肿大 D、骨质疏松.
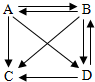 某同学画出的四种物质之间的转化关系图,A、B、C、D代表最常见的含有钠离子的四种物质的溶液,“→”表物质间的转化关系,所有的转化关系都可以通过复分解反应实现.钠离子的符号是Na+,C中溶质的化学式NaNO3 .写出A→B的化学方程式2NaOH+CO2═Na2CO3+H2O;写出D→C的化学方程式NaCl+AgNO3═AgCl↓+NaNO3 .
某同学画出的四种物质之间的转化关系图,A、B、C、D代表最常见的含有钠离子的四种物质的溶液,“→”表物质间的转化关系,所有的转化关系都可以通过复分解反应实现.钠离子的符号是Na+,C中溶质的化学式NaNO3 .写出A→B的化学方程式2NaOH+CO2═Na2CO3+H2O;写出D→C的化学方程式NaCl+AgNO3═AgCl↓+NaNO3 .