题目内容
某化学小组同学,用如图所示实验探究质量守恒定律.
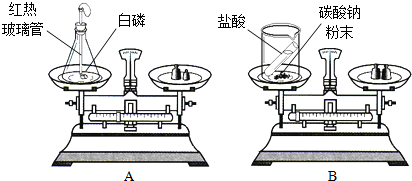
(1)实验过程中A中气球出现的现象是 ,反应的化学方程式是 .B中观察到的实验现象是 ,反应的化学方程式是 .
(2)综合分析上述2个实验,以下说法正确的是 .(填①~⑤序号)
①实验A中的气球起到了平衡瓶内外气体压强的作用
②实验A中的气球作用是收集产生的气体
③实验A中锥形瓶内事先放少量细沙的作用是防止瓶底炸裂
④实验B发生的反应不符合质量守恒定律
⑤由于实验B不是密闭体系,因此能达到实验目的只有实验A
(3)由上述实验可知,在化学反应前后,一定不变的是 (填数字序号).
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质质量
(4)红热的铁能与水蒸气反应,放出气体X,同时生成固体Y.X气体靠近火焰点火时,能燃烧或发出爆鸣声.其反应的化学方程式为:3Fe+4H2O
4X+Y.则Y的化学式为 .

(1)实验过程中A中气球出现的现象是
(2)综合分析上述2个实验,以下说法正确的是
①实验A中的气球起到了平衡瓶内外气体压强的作用
②实验A中的气球作用是收集产生的气体
③实验A中锥形瓶内事先放少量细沙的作用是防止瓶底炸裂
④实验B发生的反应不符合质量守恒定律
⑤由于实验B不是密闭体系,因此能达到实验目的只有实验A
(3)由上述实验可知,在化学反应前后,一定不变的是
①原子种类 ②原子数目 ③分子种类
④分子数目 ⑤元素种类 ⑥物质质量
(4)红热的铁能与水蒸气反应,放出气体X,同时生成固体Y.X气体靠近火焰点火时,能燃烧或发出爆鸣声.其反应的化学方程式为:3Fe+4H2O
| ||
考点:质量守恒定律的实验探究,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据白磷燃烧生成五氧化二磷,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳解答,在导管口安装气球的目的是:防止体系中的物质逸散,给实验造成误差;
(2)分析以上两个实验知;①实验A中的气球起到了平衡瓶内外气体压强的作用,说法正确;由①知,②说法不正确;③实验A锥形瓶内事先放少量细沙的作用是防止瓶底炸裂;④根据化学反应都遵守质量守恒定律解答;⑤B实验在敞开烧杯中进行,反应的过程中要生成气体,所以B肯定不平衡.
(3)化学反应前后,元素的种类不变,原子的种类、总个数不变;
(4)根据质量守恒定律可以判断物质的化学式.
(2)分析以上两个实验知;①实验A中的气球起到了平衡瓶内外气体压强的作用,说法正确;由①知,②说法不正确;③实验A锥形瓶内事先放少量细沙的作用是防止瓶底炸裂;④根据化学反应都遵守质量守恒定律解答;⑤B实验在敞开烧杯中进行,反应的过程中要生成气体,所以B肯定不平衡.
(3)化学反应前后,元素的种类不变,原子的种类、总个数不变;
(4)根据质量守恒定律可以判断物质的化学式.
解答:解:
(1)实验过程中A中,锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷熄消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;磷和氧气在点燃的条件下生成五氧化二磷,白磷燃烧的化学方程式为:4P+5O2
2P2O5;B实验中是碳酸钠和盐酸的反应,其化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(2)分析以上两个实验知;①实验A中的气球起到了平衡瓶内外气体压强的作用,说法正确;由①知,②说法不正确;③实验A锥形瓶内事先放少量细沙的作用是防止瓶底炸裂;④根据化学反应都遵守质量守恒定律解答;⑤B实验在敞开烧杯中进行,反应的过程中要生成气体,所以B肯定不平衡.
(3)在化学反应前后,
①原子种类一定不变;
②原子数目一定不变;
③分子种类一定改变;
④分子数目可能改变,也可能不改变;
⑤元素种类一定不变;
⑥物质质量一定不变.
故填:①②⑤⑥.
(4)X气体靠近火焰点火时,能燃烧或发出爆鸣声,说明X是氢气,由3Fe+4H2O
4H2+Y可知,氢原子反应前后个数相等,Y中应该含有3个铁原子和4个氧原子,是四氧化三铁,化学式是Fe3O4
答案:
(1)气球先膨胀后缩小 4P+5O2
2P2O5 烧杯中有气泡产生 Na2CO3+2HCl═2NaCl+H2O+CO2↑
(2)①③⑥
(3)①②⑤⑥
(4)Fe3O4
(1)实验过程中A中,锥形瓶中白磷燃烧放出热量,使瓶内气体急剧膨胀,所以气球先膨胀,燃烧熄灭后,冷却到室温,由于白磷熄消耗瓶内氧气,瓶内气体减少,压强减小,所以气球有变小;磷和氧气在点燃的条件下生成五氧化二磷,白磷燃烧的化学方程式为:4P+5O2
| ||
(2)分析以上两个实验知;①实验A中的气球起到了平衡瓶内外气体压强的作用,说法正确;由①知,②说法不正确;③实验A锥形瓶内事先放少量细沙的作用是防止瓶底炸裂;④根据化学反应都遵守质量守恒定律解答;⑤B实验在敞开烧杯中进行,反应的过程中要生成气体,所以B肯定不平衡.
(3)在化学反应前后,
①原子种类一定不变;
②原子数目一定不变;
③分子种类一定改变;
④分子数目可能改变,也可能不改变;
⑤元素种类一定不变;
⑥物质质量一定不变.
故填:①②⑤⑥.
(4)X气体靠近火焰点火时,能燃烧或发出爆鸣声,说明X是氢气,由3Fe+4H2O
| ||
答案:
(1)气球先膨胀后缩小 4P+5O2
| ||
(2)①③⑥
(3)①②⑤⑥
(4)Fe3O4
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
相关题目
下列各化合物中,氮元素的化合价有 显十5价的是( )
| A、N2O |
| B、N2O3 |
| C、NO2 |
| D、NH4NO3 |
 将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.
将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.