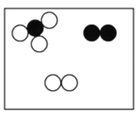
题目内容
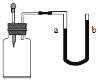
黄铜是铜和锌的合金。为了测定某黄铜中铜的质量分数,称取10.0g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时共用去98.0g稀硫酸,将反应后的剩余物过滤、干燥,称得剩余固体3.5g。试计算:
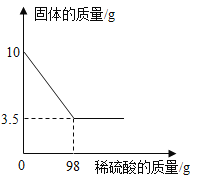
求:(1)铜样品中锌的质量是______(直接填结果);
(2)所用稀硫酸溶液的溶质质量分数是_____?(写过程)
练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
“黄铜”是铜和锌的合金,为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行实验,实验数据如下。(烧杯质量均为56.5克)
1 | 甲 | 乙 | 丙 |
烧杯+稀盐酸质量 | 98.0g | 93.0g | 93.0g |
加入黄铜样品质量 | 10.0g | 12.0g | 10.0g |
充分反应后,烧杯+剩余物质质量 | 107.9g | 104.9g | 102.9g |
请回答下列问题:
(1)_____同学用的稀盐酸和黄铜样品恰好完全反应,他制取的氢气的质量是_____。
(2)计算黄铜样品中锌的质量分数_____(要求写出计算过程)。
(3)计算盐酸的质量分数为_____。


 ”、“
”、“ ”分别表示不同元素的原子,则其中表示化合物的是
”分别表示不同元素的原子,则其中表示化合物的是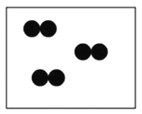 B.
B.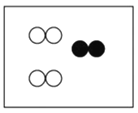 C.
C. D.
D.