题目内容
5.烧碱(NaOH)是一种重要的化工原料,广泛应用于肥皂、造纸等工业.下面有一些关于烧碱的问题,请按要求解答:(1)烧碱在工业上通常用电解饱和NaCl水溶液的方法制取,产物除烧碱外,还有H2和Cl2,请写出电解饱和NaCl水溶液的化学方程式2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑.
(2)烧碱放在空气中会变质生成碳酸钠.现有14.6g暴露在空气中的烧碱样品,全部溶于水,然后滴加足量Ca(OH)2溶液,充分反应后,过滤,烘干得10g沉淀,则样品的组成为D.
A.全部为Na2CO3
B.4gNaCO3和10.6gNaOH
C.全部为NaOH
D.4gNaOH和10.6gNa2CO3
(3)如图是某学生用氢氧化钠固体和水配制60g10%NaOH溶液的部分操作过程,该同学在称量氢氧化钠时,先在两个托盘上各放一张质量相同的纸,然后把氢氧化钠药品直接放在纸上称量.

①a操作中的错误是氢氧化钠既易潮解,又具有腐蚀性,不能放在纸上称量,要放在玻璃器皿中称量.
②下列操作中导致溶质质量分数偏低的是AB(填字母).
A.a操作中砝码和氢氧化钠放错盘
B.b中烧杯用水洗涤后未干燥就使用
C.c操作中平视量筒凹液面最低处读数为50mL
D.d操作中有少量水溅出.
(4)酸碱中和反应在工农业生产和科研上具有很大用途,但氢氧化钠溶液和盐酸反应时看不到明显现象,请你设计一个实验,通过观察到的明显现象,说明氢氧化钠溶液与盐酸发生了反应:把加有酚酞的氢氧化钠溶液滴入稀盐酸,红色消失.
(5)若中和反应需要60g10%的NaOH溶液,现提供50g20%的NaOH溶液、40g5%的NaOH溶液以及足够的NaOH固体和水,请选用以上提供的药品设计两种配制方案(只要说明配制所需的各种药品用量)填入表中.
| 序号 | 配置方案 |
| 举例 | 6gNaOH固体和54g水 |
| 方案1 | |
| 方案2 |
分析 (1)根据题目对反应的描述,确定反应的反应物与生成物,完成反应的化学方程式;
(2)根据碳酸钠与氢氧化钙生成碳酸钙沉淀和氢氧化钠的化学方程式,由生成沉淀碳酸钙的质量可计算14.6g固体中含有碳酸钠的质量,固体质量与碳酸钠质量差即为氢氧化钠的质量;
(3)①根据氢氧化钠具有腐蚀性不能放在纸上称量考虑;②根据导致溶质质量分数偏低要从两个方面考虑:称量的溶质少了,量取的水多了进行分析;
(4)借助 酸碱指示剂遇酸碱呈现不同颜色的特点,可把滴有酚酞而呈红色的氢氧化钠溶液滴入稀盐酸中,通过红色消失以证实反应的发生;
(5)根据配制60g 10%的NaOH溶液,只需要取足氢氧化钠60g×10%=6g,然后加入适量水使得溶液质量达到60g即可完成所需要溶液的配制.
解答 解:(1)电解饱和NaCl水溶液的方法制取烧碱,还可以产生H2和Cl2,因此反应的化学方程式为2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(2)设样品中碳酸钠的质量为x
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
106 100
x 10g
$\frac{106}{x}=\frac{100}{10g}$
x=10.6g
样品中NaOH的质量=14.6g-10.6g=4g
故选:D;
(3)①氢氧化钠既易潮解,又具有腐蚀性,不能放在纸上称量,要放在玻璃器皿中称量;
②A.a操作中砝码和氢氧化钠放错盘,会导致称量氢氧化钠质量偏小,会导致溶质质量分数偏低,故A正确;
B、b中烧杯用水洗涤后未干燥就使用,会导致水多了,也会使溶质质量分数偏低,故B正确;
C、应该需要水54mL,如果平视量筒凹液面最低处读数为50mL,水少了会导致溶质质量分数偏大,故C错;
D、d操作中有少量水溅出,水少了会导致溶质质量分数偏大,故D错;
故选AB;
(4)滴有酚酞的氢氧化钠的溶液呈红色,把这种呈红色的溶液滴入稀盐酸中,可观察到滴入的溶液红色立即消失,可说明氢氧化钠与盐酸发生了反应;
(5)配制60g 10%的NaOH溶液,需要氢氧化钠60g×10%=6g,因此可采取取30g 20%的NaOH溶液加入60g-30g=30g水、取40g 5%的NaOH溶液再加入6g-40g×5%=4g氢氧化钠固体和60g-40g-4g=16g水进行混合,都可得到60g 10%的NaOH溶液;
故答案为:
(1)2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
(2)D;
(3)①氢氧化钠既易潮解,又具有腐蚀性,不能放在纸上称量,要放在玻璃器皿中称量;②AB;
把加有酚酞的氢氧化钠溶液滴入稀盐酸,红色消失;
(5)
| 方案1 | 30g 20%的NaOH溶液和30g水 |
| 方案2 | 40g 5%的NaOH溶液、4g NaOH固体和16g水 |
点评 本题通过氢氧化钠这一物质综合考查了化学方程式的书写、化学方程式的计算、实验的设计及配制一定质量分数的溶液,在解答时要耐心思考.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案| A. | 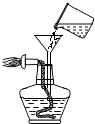 添加酒精 | B. | 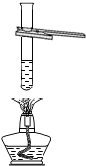 给液体加热 | C. | 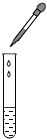 用滴管滴加溶液 | D. |  称一定量的食盐 |
| A. | 提倡长期饮用纯水(蒸馏水) | |
| B. | 使用无磷洗衣粉有利于保护水资源 | |
| C. | 水体有自净能力,未经处理的生活污水可任意排放 | |
| D. | 电解水时,负极产生的是氧气 |
| A. | NO3- H+ Na+ OH- | B. | K+ SO42- Na+ NO3- | ||
| C. | Cl- K+ SO42- Ba2+ | D. | Ca2+ Cl- CO32- K+ |
| A. | 铁丝在氧气中燃烧时,火星四射 | |
| B. | 镁条在空气中燃烧时,发出耀眼的白光 | |
| C. | 木炭在氧气中燃烧时,发出白光 | |
| D. | 硫粉在氧气中燃烧时,产生淡蓝色火焰 |

 夏天来临,户外光线变强,为零减少对眼睛的刺激,变色眼镜是成为人们常用的护眼工具.如图是一框变色眼镜的示意图:
夏天来临,户外光线变强,为零减少对眼睛的刺激,变色眼镜是成为人们常用的护眼工具.如图是一框变色眼镜的示意图: