题目内容
20.某化学兴趣小组三位同学在学习盐酸与氢氧化钠反应后,分别结合自己在实验室中所做的实验,各从不同方面对其进行图象描述.图A是实际操作图,图B是反应过程中溶液的酸碱度变化图,图C是微观粒子结合过程的示意图.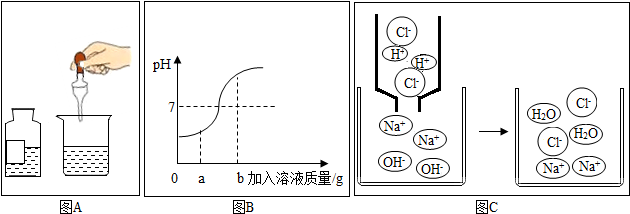
根据图B的曲线变化,回答下列问题:
(1)该变化对应的实验操作是将氢氧化钠溶液滴加到另一种溶液中;
(2)当滴入溶液的质量为ag时,溶液中的溶质为HCl、NaCl(填化学式);
(3)当溶液的pH=7时,溶液中的主要离子是Na+、Cl-(填离子符号);
(4)当加入溶液的质量为bg时,向所得溶液中滴加紫色石蕊试液,溶液是蓝色;
【结论】从反应前后离子的种类看,有些离子参与了反应,有些离子只是旁观者,该反应中参与反应的离子是氢离子;氢氧根离子.
分析 (1)根据坐标变化的趋势结合盐酸的PH小于7,氢氧化钠溶液的PH大于7分析;
(2)当加入溶液的质量为ag时,溶液呈现酸性,溶液中既有生成的氯化钠,又有未反应的盐酸;
(3)根据当溶液的pH=7时,酸碱恰好完全反应解答;
(4)当加入溶液的质量为bg时,溶液显碱性能使石蕊试液变红色.
【结论】根据中和反应的实质是酸电离的氢离子和碱电离的氢氧根离子相互作用生成水的过程,即中和反应的实质是H++OH-=H2O.
解答 解:(1)坐标的pH变化是由小于7到大于7的过渡,因此进行的操作是将氢氧化钠溶液滴加到稀盐酸中.
(2)当加入溶液的质量为ag时,溶液呈现酸性,所得溶液中的溶质为氯化氢和氯化钠.
故填:HCl、NaCl;
(3)当溶液的pH=7时,酸碱恰好完全反应,溶液中的主要离子是(些离子符号)钠离子和氯离子;
(4)当加入溶液的质量为bg时,所得溶液显碱性,能使石蕊试液变蓝色.故填:蓝.
【结论】中和反应的实质是酸电离的氢离子和碱电离的氢氧根离子相互作用生成水的过程,即中和反应的实质是H++OH-=H2O.
答案:
(1)氢氧化钠溶液;
(2)HCl、NaCl;
(3)Na+、Cl-;
(4)蓝;
【结论】氢离子;氢氧根离子.
点评 解答本题的关键是根据坐标的pH变化结合溶液的酸碱性与溶液pH的关系进行分析,并对反应过程中的溶液的酸碱性正确判断.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.下列做法或说法不合理的是( )
| A. | 使用可降解塑料制品以减少“白色污染” | |
| B. | 霉变的花生清洗后也不能食用 | |
| C. | 香肠中加入较多量的亚硝酸钠防腐 | |
| D. | 废旧报纸、废弃铝制易拉罐放入可回收垃圾箱 |
11.下列操作中,正确的是( )
| A. | 把氢氧化钠固体放在天平右盘的玻璃器皿中称量 | |
| B. | 给试管中的液体加热,液体最好不超过试管容积的$\frac{1}{2}$ | |
| C. | 过滤时,将液体沿玻璃棒慢慢向漏斗中倾倒,液面要始终低于滤纸的边缘 | |
| D. | 用胶头滴管滴加液体时,为防止液体溅出应将滴管口紧贴试管内壁 |
8.物质的性质决定其用途,下列因果关系不成立的是( )
| A. | 稀有气体化学性质稳定,可用作保护气 | |
| B. | 干冰升华吸热,可用于人工降雨 | |
| C. | 熟石灰呈碱性,可用来改良酸性土壤 | |
| D. | 稀硫酸能与金属反应,可用来除锈 |
15. 某反应前后分子变化的微观示意图如图所示,下列说法错误的是( )
某反应前后分子变化的微观示意图如图所示,下列说法错误的是( )
 某反应前后分子变化的微观示意图如图所示,下列说法错误的是( )
某反应前后分子变化的微观示意图如图所示,下列说法错误的是( )| A. | 生成物均为氧化物 | |
| B. | 甲是有机物,乙、丙、丁是无机物 | |
| C. | 点燃前,要先检验甲的纯度,防止爆炸 | |
| D. | 参加反应的甲、乙微粒个数比为1:2 |
9.运送汽油的油罐车必须悬挂的标志是( )
| A. |  | B. |  | C. |  | D. |  |
6.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂,下列有关高铁酸钠的说法正确的是( )
| A. | 属于有机化合物 | B. | 由两种金属和一种非金属组成 | ||
| C. | 铁元素的质量分数为33.73% | D. | 钠、铁、氧三种元素质量比是2:1:4 |