题目内容
1.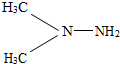 “神州”五号宇宙载人飞船飞行试验成功,标志着我国科技水平达到了一个新的高峰.运送“神州”五号宇宙飞船的火箭所用燃料为偏二甲肼.偏二甲肼的结构简式如图所示,下列说法中错误的是( )
“神州”五号宇宙载人飞船飞行试验成功,标志着我国科技水平达到了一个新的高峰.运送“神州”五号宇宙飞船的火箭所用燃料为偏二甲肼.偏二甲肼的结构简式如图所示,下列说法中错误的是( )| A. | 偏二甲肼的相对分子质量为60 | |
| B. | 偏二甲肼中碳、氢、氮三种元素的质量比1:4:1 | |
| C. | 偏二甲肼中碳元素的质量分数为40% | |
| D. | 偏二甲肼的一个分子中共有12个原子 |
分析 A.根据相对分子质量的计算方法来分析;
B.根据化合物中各元素质量比的计算方法来分析;
C.根据化合物中元素质量分数的计算方法来分析;
D.根据分子结构来分析.
解答 解:A.偏二甲肼C2H8N2的相对分子质量=12×2+1×8+14×2=60;故正确;
B.偏二甲肼C2H8N2中碳、氢、氮三种元素的质量比=(12×2):(1×8):(14×2)=6:2:7≠1:4:1;故错误;
C.偏二甲肼中碳元素的质量分数为$\frac{12×2}{60}×100%$=40%,故正确;
D.每个偏二甲肼分子中含2个C原子、8个H原子和2个N原子,共12个原子,故正确.
故选B.
点评 本题主要考查学生运用所学化学知识解决实际问题的能力,透彻理解教材内容是解决问题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.如图所示的是郑亮同学设计的利用一氧化碳还原氧化铁的实验装置,请根据题目要求回答下列问题.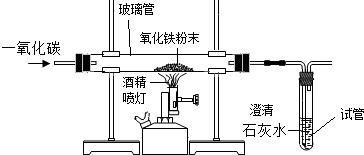
(1)写出用一氧化碳还原氧化铁的化学反应方程式.Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(2)老师觉得郑亮设计的方案有一定的缺陷.请你将这一缺陷写在下面的横线上.缺少尾气处理装置
(3)请在表中将实验过程所涉及的实验现象补充完整.
(4)请用化学反应方程式解释试管中该现象产生的原因.CO2+Ca(OH)2=CaCO3↓+H2O.

(1)写出用一氧化碳还原氧化铁的化学反应方程式.Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(2)老师觉得郑亮设计的方案有一定的缺陷.请你将这一缺陷写在下面的横线上.缺少尾气处理装置
(3)请在表中将实验过程所涉及的实验现象补充完整.
| 装置 | 实验现象 |
| 玻璃管 | 红色粉末变成黑色 |
| 试管 | 澄清的石灰水变浑浊 |
13.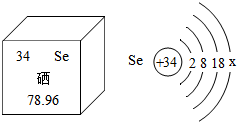 硒是人体生命活动中必需的微量元素之一,是人体内的抗氧化剂,能提高人体免疫力,具有多种生物功能,硒被誉为“抗癌大王”.如图提供了硒的有关信息,下列说法中,正确的是( )
硒是人体生命活动中必需的微量元素之一,是人体内的抗氧化剂,能提高人体免疫力,具有多种生物功能,硒被誉为“抗癌大王”.如图提供了硒的有关信息,下列说法中,正确的是( )
 硒是人体生命活动中必需的微量元素之一,是人体内的抗氧化剂,能提高人体免疫力,具有多种生物功能,硒被誉为“抗癌大王”.如图提供了硒的有关信息,下列说法中,正确的是( )
硒是人体生命活动中必需的微量元素之一,是人体内的抗氧化剂,能提高人体免疫力,具有多种生物功能,硒被誉为“抗癌大王”.如图提供了硒的有关信息,下列说法中,正确的是( )| A. | 硒的相对原子质量是78.96,硒属于金属元素 | |
| B. | 硒原子序数和原子核内中子数均为34 | |
| C. | 硒原子和硫原子化学性质相似,其Se2-的核外电子数为36 | |
| D. | 硒元素对人体有那么多的好处,其补充多多益善 |
10.二氧化钛[TiO2]中钛元素的化合价为( )
| A. | -2 | B. | +2 | C. | +3 | D. | +4 |
11.科学研究发现:金星大气层的成分之一是三氧化二碳(C2O3),实验证明三氧化二碳的化学性质与一氧化碳相似.下列关于三氧化二碳的说法中,不正确的是( )
| A. | C2O3能使澄清石灰水变浑浊 | B. | C2O3的密度比空气的密度大 | ||
| C. | C2O3在一定条件下能还原氧化铁 | D. | C2O3在O2中充分燃烧的产物为CO2 |

 如图是实验室制取气体的常用装置.
如图是实验室制取气体的常用装置.