题目内容
4.写出一种除去下列物质中的杂质(括号内物质)的试剂的化学式:硝酸钾(氯化钾)AgNO3; 氯化镁(硫酸镁)BaCl2.
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:要除去硝酸钾溶液中的氯化钾,实质就是除去氯离子,可利用氯化钾溶液与适量的硝酸银溶液反应生成氯化银淀和硝酸钾溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则.
要除去氯化镁溶液中的硫酸镁,实质就是除去硫酸根离子,可利用硫酸镁溶液与适量的氯化钡溶液反应生成硫酸钡沉淀和氯化镁溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则.
故答案为:AgNO3;BaCl2.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案
相关题目
14.医用泻盐的主要成分是MgSO4,其物质类别属于( )
| A. | 酸 | B. | 碱 | C. | 盐 | D. | 氧化物 |
12.春节期间小明对当地雨水的酸碱度进行了检测.他将收集的雨水,每隔5min用pH计检测一次,其pH值如表.
(1)为了判断雨水酸度是否正常,他做了如下对比试验:将足量CO2气体通入蒸馏水中,检测所得溶液的pH为5.60,有关反应的化学方程式为CO2++H2O=H2CO3 .据此得出,他收集的雨水是否为酸雨?是(填“是”或“否”).在检测的期间,雨水的酸度随着时间的变化逐渐增强(填“增强”或“减弱”).
(2)经调查,近几天空气中SO2、NO2含量明显增多,小明很那纳闷;春节期间,工厂大多停产、运输车辆也比往日减少,空气中SO2、NO2怎么会增多呢?耳边鸣响的鞭炮声使他恍然大悟,鞭炮爆炸会产生SO2、NO2等污染物,小明通过查询资料得知,SO2(含NO2)的化学性质与CO2相似.他设计用氢氧化钠溶液来吸收鞭炮爆炸时产生的SO2(含NO2),情写出有关的化学方程式SO2+2NaOH═Na2SO3+H2O.
(3)通过小明的实验,你作为一名有一定科学素养的中学生,如何看待燃放鞭炮这一现象?
| 测定时间 | 8:05 | 8:10 | 8:15 | 8:20 | 8:25 | 8:30 |
| pH | 4.94 | 4.92 | 4.90 | 4.88 | 4.86 | 4.85 |
(2)经调查,近几天空气中SO2、NO2含量明显增多,小明很那纳闷;春节期间,工厂大多停产、运输车辆也比往日减少,空气中SO2、NO2怎么会增多呢?耳边鸣响的鞭炮声使他恍然大悟,鞭炮爆炸会产生SO2、NO2等污染物,小明通过查询资料得知,SO2(含NO2)的化学性质与CO2相似.他设计用氢氧化钠溶液来吸收鞭炮爆炸时产生的SO2(含NO2),情写出有关的化学方程式SO2+2NaOH═Na2SO3+H2O.
(3)通过小明的实验,你作为一名有一定科学素养的中学生,如何看待燃放鞭炮这一现象?
9.下列实验操作正确的是( )
| A. | 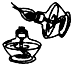 点燃酒精灯 | B. | 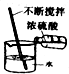 稀释浓硫酸 | C. | 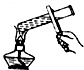 加热液体 | D. |  倾倒液体 |
13.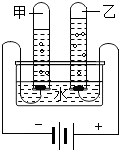 用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )
用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )
 用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )
用如图装置进行电解水实验,有以下描述:①向水中加入少量的硫酸,能使水电解产生气体的速度变快;②甲、乙两试管内收集到的气体的体积比约为2:1; ③甲试管内产生的气体能燃烧;④乙试管内的气体具有可燃性.以上描述中正确的是( )| A. | ①②③④ | B. | ①② | C. | ①②③ | D. | ②③ |
14.某温度时,固体A的溶解度为25g.则在该温度下,A的饱和溶液中,溶质质量(a)、溶剂质量(b)和溶液质量(c)具有的关系是( )
| A. | c:b=4:5 | B. | a:c=l:5 | C. | a:b=l:3 | D. | b:c=3:4 |