题目内容
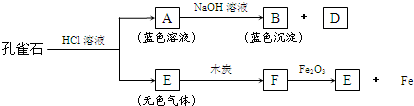
孔雀石能发生如下图所示变化: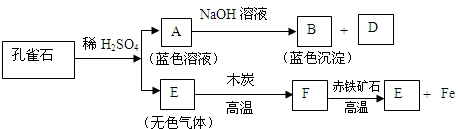
(1)A、B、D、E是何种物质,写出它们的化学式:
A
(2)从图中转化关系可以初步推断,孔雀石中含有的元素有
(3)某钢铁厂每天需消耗5000t含Fe2O376%的赤铁矿石来冶炼生铁,试计算:
①该5000t赤铁矿中含Fe2O3的质量为多少?
②该厂理论上可日产含铁98%的生铁的质量是多少?(计算结果保留一位小数)
分析:(1)由关系图,根据颜色,蓝色沉淀B可确定为氢氧化铜,蓝色溶液A为硫酸铜;由F与赤铁矿可生成铁和气体E,可确定F为一氧化碳、E为二氧化碳;根据以上分析可完成对其它物质的判断;
(2)根据孔雀石与硫酸反应的生成物,根据质量守恒定律及反应规律,可对孔雀石的组成中可能含有的元素做出判断;
(3)利用赤铁矿中氧化铁的质量分数及矿石质量可计算氧化铁的质量;根据冶炼过程中铁的质量不变,可由氧化铁中所含量铁的质量计算日产含铁98%的生铁的质量.
(2)根据孔雀石与硫酸反应的生成物,根据质量守恒定律及反应规律,可对孔雀石的组成中可能含有的元素做出判断;
(3)利用赤铁矿中氧化铁的质量分数及矿石质量可计算氧化铁的质量;根据冶炼过程中铁的质量不变,可由氧化铁中所含量铁的质量计算日产含铁98%的生铁的质量.
解答:解:(1)根据颜色,蓝色沉淀B可确定为氢氧化铜,蓝色溶液A为硫酸铜;由关系图,A物质硫酸铜与氢氧化钠反应生成B沉淀氢氧化铜和D物质硫酸钠;由F与赤铁矿可生成铁和气体E,可确定F为一氧化碳、E为二氧化碳;
综上所述,物质A为CuSO4;物质B为Cu(OH)2;物质D为Na2SO4;气体E为CO2;
(2)由于孔雀石能与硫酸反应生成硫酸铜并放出二氧化碳,可判断孔雀石中含铜元素和碳酸根,因此,孔雀石中含有的元素有Cu、C、O;
(3)①5000t赤铁矿中含Fe2O3的质量=5000t×76%=3800t
②解法一:3800tFe2O3中铁元素的质量=3800t×
×100%=2660t
日产含铁98%的生铁的质量=2660t÷98%=2714.3t
解法二:设可生产铁的质量为x
Fe2O3+3CO
3CO2↑+2Fe
160 112
3800t x
=
,x=2660t
生铁的质量=2660t÷98%=2714.3t
故答案为:
(1)CuSO4;Cu(OH)2;Na2SO4;CO2;
(2)Cu、C、O(铜元素、碳元素和氧元素);
(3)①该5000t赤铁矿中含Fe2O3的质量为3800t;②该厂理论上可日产含铁98%的生铁的质量是2714.3t.
综上所述,物质A为CuSO4;物质B为Cu(OH)2;物质D为Na2SO4;气体E为CO2;
(2)由于孔雀石能与硫酸反应生成硫酸铜并放出二氧化碳,可判断孔雀石中含铜元素和碳酸根,因此,孔雀石中含有的元素有Cu、C、O;
(3)①5000t赤铁矿中含Fe2O3的质量=5000t×76%=3800t
②解法一:3800tFe2O3中铁元素的质量=3800t×
| 56×2 |
| 160 |
日产含铁98%的生铁的质量=2660t÷98%=2714.3t
解法二:设可生产铁的质量为x
Fe2O3+3CO
| ||
160 112
3800t x
| 160 |
| 3800t |
| 112 |
| x |
生铁的质量=2660t÷98%=2714.3t
故答案为:
(1)CuSO4;Cu(OH)2;Na2SO4;CO2;
(2)Cu、C、O(铜元素、碳元素和氧元素);
(3)①该5000t赤铁矿中含Fe2O3的质量为3800t;②该厂理论上可日产含铁98%的生铁的质量是2714.3t.
点评:在利用化学方程式计算日产生铁质量时,需要注意根据反应化学方程式所计算出的铁为纯净物铁的质量而非生铁这种混合物的质量,因为化学方程式的计算中所涉及物质的质量都是纯净物的质量.

练习册系列答案
相关题目
孔雀石能发生如下图所示变化:
|
|
① 推断A、B、D、E是何种物质,写出它们的化学式:
A ,B ,D ,E 。
② 从图中转化关系可以初步判断,孔雀石中含有的元素是 。
③ F跟Fe2O3反应的化学方程式是 ,在该反应中作还原剂的是 。
 ,它的原子核内有
,它的原子核内有