题目内容
小刚在化学实验室发现,盛放氢氧化钠的试剂瓶瓶口和橡胶塞上出现了白色粉末.小刚叫来小军和小红,共同探讨这种白色粉末的成分.他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:
①可能是氢氧化钠,②可能是碳酸钠 ③可能是 .为了验证猜想,他们分别作了如下实验.
(1)小刚取少量白色粉末,滴加稀盐酸,有气体生成.由此小刚认为白色粉末是碳酸钠.请判断小刚的理论是否正确,并简述理由. .
(2)小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色.由此小军认为白色粉末是氢氧化钠.请判断小军的理论是否正确,并简述理由. .
(3)小红取少量白色粉末溶于水,向所得溶液中滴加氯化钡试液,有白色沉淀产生.由此判断白色粉末中含有 .为了验证猜想③,小红继续向溶液中滴加氯化钡试液至不再产生沉淀,然后过滤.你认为他接下来还应进行的实验是 .
在小红所做的实验中,若把氯化钡换成氢氧化钡溶液是否可行?请简述理由. .
①可能是氢氧化钠,②可能是碳酸钠 ③可能是
(1)小刚取少量白色粉末,滴加稀盐酸,有气体生成.由此小刚认为白色粉末是碳酸钠.请判断小刚的理论是否正确,并简述理由.
(2)小军取少量白色粉末溶于水,向所得溶液中滴加酚酞试液,溶液变为红色.由此小军认为白色粉末是氢氧化钠.请判断小军的理论是否正确,并简述理由.
(3)小红取少量白色粉末溶于水,向所得溶液中滴加氯化钡试液,有白色沉淀产生.由此判断白色粉末中含有
在小红所做的实验中,若把氯化钡换成氢氧化钡溶液是否可行?请简述理由.
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质
专题:科学探究
分析:根据部分变质来考虑;(1)加入盐酸有气泡只能说明有碳酸钠存在,不能说明白色粉末就是碳酸钠;(2)根据碳酸钠的碱性考虑;(3)根据碳酸钠与氯化钡反应的生成物考虑,根据见能使酚酞试液变红考虑是否含有氢氧化钠.
解答:解:白色粉末全部是氢氧化钠,说明没变质,全部是碳酸钠说明全部变质,如果部分变质说明既有没变质的氢氧化钠,又有变质的碳酸钠;
(1)加入盐酸有气泡只能说明有碳酸钠存在,不能说明白色粉末就是碳酸钠,NaOH和Na2CO3 的混合物加入盐酸也能产生气泡;
(2)因为碳酸钠虽然属于盐,但显碱性也能使酚酞试液变红,所以向其中滴加酚酞试液,溶液变为红色,判断白色粉末为氢氧化钠是错误的;
(3)由于氢氧化钠与氯化钡不反应,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,所以滴加氯化钡溶液,有白色沉淀产生,说明含有碳酸钠;向溶液中滴加氯化钡溶液,至不再产生沉淀,主要是除去混合物中的碳酸钠,因为碳酸钠虽然属于盐,但显碱性也能使酚酞试液变红,除去碳酸钠生成的氯化钠显中性,再加入酚酞变红说明含有氢氧化钠,不变红说明不含有氢氧化钠;如果加入氢氧化钡后,氢氧化钡与碳酸钠反应生成碳酸钡沉淀和氢氧化钠,就无法验证原来混合物中是否含有氢氧化钠了.
故答案为:NaOH和Na2CO3 的混合物;
(1)不正确;NaOH和Na2CO3 的混合物加入盐酸也能产生气泡;
(2)不正确;碳酸钠溶液显碱性,也能使酚酞试液变红色;
(3)Na2CO3 ;向滤液中加入无色酚酞试液;不行;如果加入氢氧化钡后,氢氧化钡与碳酸钠反应生成碳酸钡沉淀和氢氧化钠,就无法验证原来混合物中是否含有氢氧化钠了.
(1)加入盐酸有气泡只能说明有碳酸钠存在,不能说明白色粉末就是碳酸钠,NaOH和Na2CO3 的混合物加入盐酸也能产生气泡;
(2)因为碳酸钠虽然属于盐,但显碱性也能使酚酞试液变红,所以向其中滴加酚酞试液,溶液变为红色,判断白色粉末为氢氧化钠是错误的;
(3)由于氢氧化钠与氯化钡不反应,碳酸钠与氯化钡反应生成碳酸钡沉淀和氯化钠,所以滴加氯化钡溶液,有白色沉淀产生,说明含有碳酸钠;向溶液中滴加氯化钡溶液,至不再产生沉淀,主要是除去混合物中的碳酸钠,因为碳酸钠虽然属于盐,但显碱性也能使酚酞试液变红,除去碳酸钠生成的氯化钠显中性,再加入酚酞变红说明含有氢氧化钠,不变红说明不含有氢氧化钠;如果加入氢氧化钡后,氢氧化钡与碳酸钠反应生成碳酸钡沉淀和氢氧化钠,就无法验证原来混合物中是否含有氢氧化钠了.
故答案为:NaOH和Na2CO3 的混合物;
(1)不正确;NaOH和Na2CO3 的混合物加入盐酸也能产生气泡;
(2)不正确;碳酸钠溶液显碱性,也能使酚酞试液变红色;
(3)Na2CO3 ;向滤液中加入无色酚酞试液;不行;如果加入氢氧化钡后,氢氧化钡与碳酸钠反应生成碳酸钡沉淀和氢氧化钠,就无法验证原来混合物中是否含有氢氧化钠了.
点评:解答本题关键是要知道碳酸钠显碱性,也能使酚酞试液变红色,只有先把碳酸钠除掉才能再加入酚酞试液,验证是否含有氢氧化钠.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法中正确的是( )
| A、食盐与水混合得到食盐水属于化合反应 |
| B、有氧气参加的反应一定是化合反应 |
| C、化合反应可能是物理变化 |
| D、氧化反应一定是化学变化 |
 如图是其品牌补铁剂的标签,请回答:
如图是其品牌补铁剂的标签,请回答:
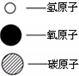



 已知空气的主要成分示氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图:
已知空气的主要成分示氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图: