题目内容
16.现有氧化镁、氢氧化镁和硫酸镁的混合物10克,加入100克9.8%的稀硫酸恰好完全反应,反应结束后蒸发,所得硫酸镁的质量可能是( )| A. | 16克 | B. | 16.5克 | C. | 17.5克 | D. | 18克 |
分析 可以根据质量守恒定律,依据硫酸根的质量求出生成硫酸镁的质量;再利用极值法确定所得硫酸镁的质量.
解答 解:氧化镁、氢氧化镁与硫酸反应后都生成硫酸镁,反应前后硫酸根的质量不变,硫酸的质量为:100g×9.8%=9.8g,
硫酸根的质量为:9.8g×$\frac{96}{98}$×100%=9.6g
设生成硫酸镁的质量为X,则有:
X×$\frac{96}{120}$×100%=9.6g,
X=12g.
当与稀硫酸反应的全部是氧化镁时,设氧化镁的质量为m,则有:
MgO→MgSO4
40 120
m 12g
$\frac{40}{120}=\frac{m}{12g}$
m=4g;
故混合物中硫酸镁的质量为:10g-4g=6g;所得硫酸镁的质量:12g+6g=18g;
当与稀硫酸反应的全部是氢氧化镁时,设氢氧化镁的质量为n,则有:
Mg(OH)2→MgSO4
58 120
n 12g
$\frac{58}{120}=\frac{n}{12g}$
mn=5.8g,
故混合物中硫酸镁的质量为:10g-5.8g=4.2g;所得硫酸镁的质量:4.2g+12g=16.2g;
因为混合物10g是氧化镁、氢氧化镁和硫酸镁的混合物,故所得硫酸铜的质量:16.2g~18g之间;
故选BC.
点评 本题主要考查了质量守恒定律方面的内容.可以依据题干提供的数据进行计算.

练习册系列答案
相关题目
6.下列常见化肥中,属于复合肥料的是( )
| A. | K2SO4 | B. | CO(NH2)2 | C. | Ca(H2PO4)2 | D. | KNO3 |
7.下列实验现象描述正确的是( )
| A. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 红磷在空气中燃烧,产生大量白雾 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色的四氧化三铁 | |
| D. | 向氢氧化钠溶液中滴入氯化铁溶液,产生红褐色沉淀 |
11.除去下列各组物质中的少量杂质,所选试剂或方法正确的是( )
| 选顼 | 物质 | 杂质(少量) | 试剂或方法 |
| A | H20 | 色素 | 活性炭 |
| B | Mn02 | KCl | 溶解、过滤、洗涤、烘干 |
| C | N2 | 02 | 通过红热的木炭 |
| D | C02 | CO | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
8.下列所示的实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
5.元素周期表是学习和研究化学的重要工具,根据如图,判断正确的是( )
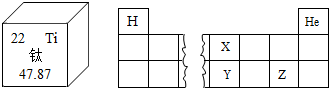

| A. | 钛元素的相对原子质量为47.87g | B. | 钛元素的核内中子数为22 | ||
| C. | Z的原子序数小于X | D. | Z和Y处于同一周期 |