题目内容
1.某化学兴趣小组用CuSO4,ZnSO4,H2SO4的混合溶液和金属X探究金属的活动性顺序,小组同学设计了如下实验,已知滤液呈浅绿色.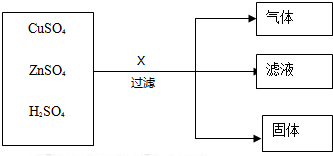
(1)Cu,Zn,H,X的活动性由强到弱的顺序是Zn>Fe>H>Cu;
(2)若向滤出的固体中加入稀盐酸,有气泡冒出,则滤液中一定含有哪些溶质(写具体物质的化学式)?请写出该过程中发生反应的化学方程式(写出一个即可)
分析 (1)根据“滤液呈浅绿色”,则推测X为铁,故可推测Cu,Zn,H,X的活动性强弱;
(2)根据“若向滤出的固体中加入稀盐酸,有气泡冒出”,则说明铁过量,因为铁与ZnSO4不反应,则推测滤液中一定含有的溶质为FeSO4,ZnSO4,
解答 解:
(1)根据“滤液呈浅绿色”,则推测X为铁,故可推测Cu,Zn,H,X的活动性强弱为Zn>Fe>H>Cu;
(2)根据“若向滤出的固体中加入稀盐酸,有气泡冒出”,则说明铁过量,铁与稀盐酸溶液反应生成FeCl2和氢气.因为Zn>Fe>H>Cu,则可知铁与ZnSO4不反应,而铁与CuSO4溶液反应生成FeSO4和铜,铁与H2SO4溶液反应生成FeSO4和氢气,则推测滤液中一定含有的溶质为FeSO4,ZnSO4;
反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu;
故答案为:
(1)Zn>Fe>H>Cu;
(2)FeSO4,ZnSO4;Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu;
点评 本题难度不大,主要考查了对金属活动性顺序的应用,利用金属活动性顺序来验证金属的活动性强弱.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
11.某三价金属的氧化物中,金属元素和氧元素的质量比9:8,则该金属的原子量为( )
| A. | 40 | B. | 56 | C. | 27 | D. | 24 |
9.某硫酸铜饱和溶液的质量分数为a%,取一定量此饱和溶液,加入w g无水CuSO4,在温度不变的情况下,析出mg 胆矾(CuSO4•5H2O)晶体,则从原饱和溶液中析出CuSO4的质量为( )
| A. | m×a% g | B. | (m-w) g | C. | (m-w)×a% g | D. | ( m+w)×a% g |
10.下列关于CO2和CO的说法,正确的是( )
| A. | CO2和CO都可用于灭火 | |
| B. | 二者组成元素相同,化学性质也相同 | |
| C. | CO2能使澄清石灰水变浑浊 | |
| D. | CO还原氧化铁的实验中,不需要进行尾气处理 |
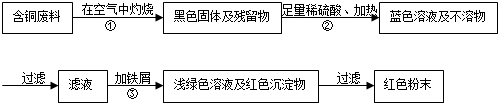
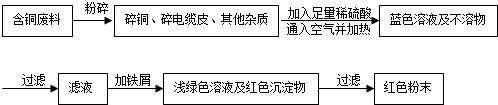
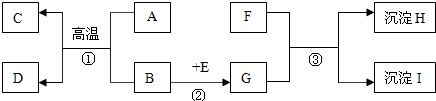
 回忆教科书中有关“粗盐中难溶性杂质的去除”实验的主要步骤,回答有关问题:
回忆教科书中有关“粗盐中难溶性杂质的去除”实验的主要步骤,回答有关问题: