题目内容
9.如图是几种粒子的结构示意图: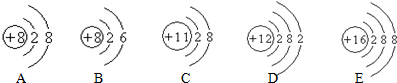
(1)A~E共有4种元素,B所表示的元素位于元素周期表的第2周期,该元素的原子容易得到(填“得到”或“失去”)电子.
(2)表示原子的粒子有BD(填序号,下同);
(3)表示阴离子的有AE;
(4)表示阳离子的有C;
(5)表示相对稳定结构的是ACE;
(6)在化学反应中易失去电子的粒子是D,形成的离子符号是Mg2+.
分析 原子结构示意图中,原子核外的电子层数等于元素周期数.质子数决定元素种类,质子数相同则属于同一种元素.最外层电子数达到8个电子时,达到相对稳定结构.
解答 解:(1)从图中可看出有4种质子数,所以有四种元素.B原子核外有2个电子层,所以B在第二周期.且最外层有6个电子,在发生化学变化时易得到电子.
(2)原子中质子数等于电子数,所以表示原子的是BD.
(3)阴离子中,质子数小于电子数,所以表示阴离子的是AE.
(4)阳离子中,质子数大于电子数,所以表示阳离子的是C.
(5)最外层电子数达到8个电子时,达到相对稳定结构.
(6)最外层电子数小于4个的,发生化学变化时,易失去电子,D中最外层电子数为2,易失去电子,形成的离子符号是Mg2+.
故答案为:
(1)4;2;得到.
(2)BD.
(3)AE.
(4)C.
(5)ACE.
(6)D;Mg2+.
点评 最外层电子数决定元素的化学性质.最外层电子数小于4个时,易失去最外层电子,达到8个电子的稳定结构.最外层电子数大于等于4个时,易得到电子达到8个电子的稳定结构.

练习册系列答案
 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
19.下列说法正确的是( )
| A. | 物质和氧气发生的反应一定属于化合反应 | |
| B. | 化学式CO2可以代表一个二氧化碳分子,也可以代表二氧化碳这种物质 | |
| C. | 原子一定是由质子、中子、电子构成的 | |
| D. | pH>7的溶液一定是碱的溶液 |
17.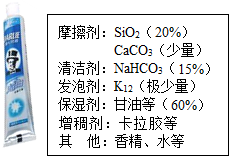 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
【资料卡片】:
a、SiO2不溶于水、且不与酸反应,高温不分解;
b、NaHCO3受热易分解,生成Na2CO3、H2O、CO2;
c、牙膏中保湿剂、增稠剂、香精等均为有机物.
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得其上层清液的pH为8.3,则此牙膏显弱碱性性,实验室能否用pH试纸测得该数值,请你作出判断并说明理由.不能,因为pH试纸只能测定出整数值;
(2)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的K12(一种钠盐)析出,则K12的溶解度和温度的关系是K12的溶解度随温度降低而降低(或随温度升高而增大);
(3)为测定此牙膏中SiO2的质量分数,兴趣小组同学设计了如下方案,并进行了3次实验:
【实验步骤】:
①准确称取2.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀HCl,至气体不再产生为止;
③过滤、洗涤、称量得到剩余固体质量(如表);
④根据实验数据进行计算.
【数据处理】:
(4)此测定做3次实验的目的是提高实验的精确度(或可信度);
(5)综合上述实验方案及实验数据,计算此牙膏中SiO2的质量分数.22%;
【实验分析】:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)高温加热的目的除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)步骤②中,加稀HCl发生的反应有CaO+2HCl═CaCl2+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(9)步骤③中,洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液;若不洗涤,则测定结果将偏大.(填“偏大”、“偏小”或“不变”)
(10)为保证洗涤效果,最好用A洗涤.
A.蒸馏水 B.自来水 C.饱和NaCl溶液 D.饱和CaCl2溶液.
 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:【资料卡片】:
a、SiO2不溶于水、且不与酸反应,高温不分解;
b、NaHCO3受热易分解,生成Na2CO3、H2O、CO2;
c、牙膏中保湿剂、增稠剂、香精等均为有机物.
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得其上层清液的pH为8.3,则此牙膏显弱碱性性,实验室能否用pH试纸测得该数值,请你作出判断并说明理由.不能,因为pH试纸只能测定出整数值;
(2)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的K12(一种钠盐)析出,则K12的溶解度和温度的关系是K12的溶解度随温度降低而降低(或随温度升高而增大);
(3)为测定此牙膏中SiO2的质量分数,兴趣小组同学设计了如下方案,并进行了3次实验:
【实验步骤】:
①准确称取2.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀HCl,至气体不再产生为止;
③过滤、洗涤、称量得到剩余固体质量(如表);
| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 试验后(g) | 0.43 | 0.44 | 0.45 |
【数据处理】:
(4)此测定做3次实验的目的是提高实验的精确度(或可信度);
(5)综合上述实验方案及实验数据,计算此牙膏中SiO2的质量分数.22%;
【实验分析】:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)高温加热的目的除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)步骤②中,加稀HCl发生的反应有CaO+2HCl═CaCl2+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(9)步骤③中,洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液;若不洗涤,则测定结果将偏大.(填“偏大”、“偏小”或“不变”)
(10)为保证洗涤效果,最好用A洗涤.
A.蒸馏水 B.自来水 C.饱和NaCl溶液 D.饱和CaCl2溶液.
14.下列模型能表示氧气分子结构的是( )
| A. | 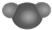 | B. |  | C. | 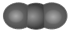 | D. | 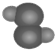 |
4.东营市公交系统目前已经推广使用节能减排的双燃料公交车.下图为公交系车燃料主要成分完全燃烧的化学反应的微观示意图.下列说法不正确的是( )
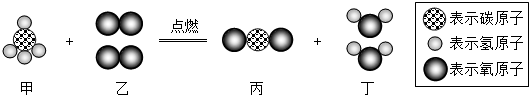

| A. | 甲是天然气的主要成分 | B. | 反应前后原子的种类和数目都不变 | ||
| C. | 该反应属于置换反应 | D. | 该反应置换的生成物都是氧化物 |
5.某校学生用化学知识解决生活中的问题,下列家庭小实验不合理的是( )
| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 用灼烧并闻气味的方法区别纯棉织物和纯毛织物 | |
| C. | 用食用碱(Na2CO3)除去面团因发酵产生的酸味 | |
| D. | 用米汤检验含碘盐中的碘酸钾(KIO3) |
 今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.
今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.