题目内容
下列各组离子能在氯化钠溶液中大量共存的是( )
| A、Ag+、Cu2+、SO42- |
| B、K+、Ba2+、NO3- |
| C、Zn2+、Na+、CO32- |
| D、Ba2+、NH4+、OH- |
考点:离子或物质的共存问题
专题:物质的分离、除杂、提纯与共存问题
分析:根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能共存,据此进行分析判断即可.
解答:解:A、氯化钠中的Cl-和Ag+形成AgCl沉淀,不符合离子大量共存的条件,不能大量共存;
B、三种离子之间在氯化钠溶液中既不能形成气体也不能产生沉淀和水,符合离子大量共存的条件,能大量共存;
C、Zn2+和CO32-形成ZnCO3沉淀,不符合离子大量共存的条件,不能大量共存;
D、NH4+和OH-可以产生气体NH3和水,不符合离子大量共存的条件,不能大量共存;
故选:B.
B、三种离子之间在氯化钠溶液中既不能形成气体也不能产生沉淀和水,符合离子大量共存的条件,能大量共存;
C、Zn2+和CO32-形成ZnCO3沉淀,不符合离子大量共存的条件,不能大量共存;
D、NH4+和OH-可以产生气体NH3和水,不符合离子大量共存的条件,不能大量共存;
故选:B.
点评:本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列关于实验现象的描述,错误的是( )
| A、镁条在氧气中燃烧,火星四射,生成黑色固体 |
| B、磷在氧气中燃烧,产生大量白烟 |
| C、硫在氧气中燃烧,火焰呈明亮的蓝紫色,生成有刺激性气味的气体 |
| D、木柴在氧气中燃烧发出白光而在空气中燃烧则呈红色的灼热状 |
下列各组物质能在pH=12的溶液中能大量共存的是( )
| A、Na2CO3、NaOH、CaCl2 |
| B、CaCl2、NaCl、KNO3 |
| C、NaOH、Na2SO4、H2SO4 |
| D、NaNO3、FeCl3、CuSO4 |
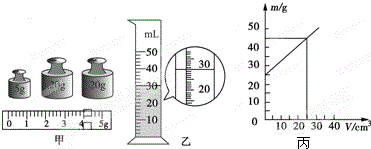 为确定某种未知液体的“身份”,科学教师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下:
为确定某种未知液体的“身份”,科学教师把这个任务交给了小明的实验小组,他们利用天平和量筒进行了多次测量.某次的操作如下: