题目内容
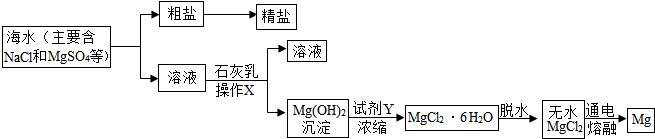
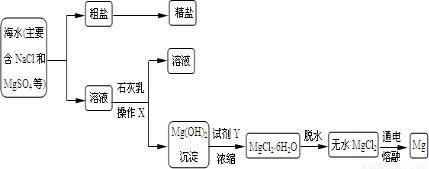
镁及其合金是一种用途广泛的金属材料,目前世界上60%的镁是从海水中提取,主要步骤如下:

请回答:
(1)实验室将粗盐制成精盐的过程中,需要蒸发,为了得到精盐应蒸发至
A、完全蒸干时停止加热
B、快干时停止加热,利用余热蒸干
C、有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(2)写出加入石灰乳的化学方程式:
(3)操作X的名称为
(4)试剂Y和Mg(OH)2反应的方程式为

请回答:
(1)实验室将粗盐制成精盐的过程中,需要蒸发,为了得到精盐应蒸发至
C
C
(填字母).A、完全蒸干时停止加热
B、快干时停止加热,利用余热蒸干
C、有大量固体析出时停止加热,过滤弃去剩余的少量溶液
(2)写出加入石灰乳的化学方程式:
Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2
Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2
.(3)操作X的名称为
过滤
过滤
,MgCl2?6H2O脱水的反应类型为分解反应
分解反应
.(4)试剂Y和Mg(OH)2反应的方程式为
2HCl+Mg(OH)2═MgCl2+2H2O
2HCl+Mg(OH)2═MgCl2+2H2O
,无水MgCl2在熔融状态下通电生成Mg的化学方程式为MgCl2(熔融)
Mg+Cl2↑
| ||
MgCl2(熔融)
Mg+Cl2↑
.
| ||
分析:(1)可根据实验室将粗盐制成精盐的过程中,蒸发停止的时机来分析;
(2)正确书写氢氧化钙溶液和氯化镁反应的化学方程式;
(3)可根据Mg(OH)2沉淀不溶于水,可用过滤的方法分离,回顾基本反应类型的特点;
(4)根据题目信息来解答,找准反应物、生成物和反应条件,正确书写化学方程式.
(2)正确书写氢氧化钙溶液和氯化镁反应的化学方程式;
(3)可根据Mg(OH)2沉淀不溶于水,可用过滤的方法分离,回顾基本反应类型的特点;
(4)根据题目信息来解答,找准反应物、生成物和反应条件,正确书写化学方程式.
解答:解:(1)实验室将粗盐制成精盐的过程中,需要蒸发,为了得到精盐应蒸发至有大量固体析出时停止加热,过滤弃去剩余的少量溶液,故选C;
(2)加入石灰乳的化学方程式:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;
(3)因Mg(OH)2沉淀不溶于水,可用过滤的方法分离,故答案为:过滤;MgCl2?6H2O脱水的反应类型为 分解反应.
(4)Mg(OH)2与HCl反应生成了MgCl2和H2O,方程式为:Mg(OH)2+2HCl=MgCl2+H2O;无水MgCl2在熔融状态下,通电后会产生Mg和Cl2:MgCl2(熔融)
Mg+Cl2↑.
故答案为:(1)C.(2)Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
(3)过滤,分解反应.(4)2HCl+Mg(OH)2═MgCl2+2H2O,MgCl2(熔融)
Mg+Cl2↑
(2)加入石灰乳的化学方程式:Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2;
(3)因Mg(OH)2沉淀不溶于水,可用过滤的方法分离,故答案为:过滤;MgCl2?6H2O脱水的反应类型为 分解反应.
(4)Mg(OH)2与HCl反应生成了MgCl2和H2O,方程式为:Mg(OH)2+2HCl=MgCl2+H2O;无水MgCl2在熔融状态下,通电后会产生Mg和Cl2:MgCl2(熔融)
| ||
故答案为:(1)C.(2)Ca(OH)2+MgCl2=Mg(OH)2↓+CaCl2.
(3)过滤,分解反应.(4)2HCl+Mg(OH)2═MgCl2+2H2O,MgCl2(熔融)
| ||
点评:本题主要考查了从海水中提取镁的过程,难度不大,掌握提取的原理是解题的关键.

练习册系列答案
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目