题目内容
5.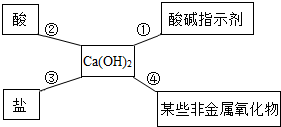 对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应.
对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应.(1)为了验证氢氧化钙将无色酚酞试液滴入氢氧化钙溶液中,溶液由无色变红色.
(2)利用氢氧化钙与盐反应的性质,可以除去氢氧化钠溶液中少量的氢氧化钙杂质,请写出该化学反应的方程式Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
分析 (1)根据酚酞溶液遇酸性溶液不变色,遇碱性溶液变红色,进行分析解答.
(2)除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)氢氧化钙溶液显碱性,将无色酚酞试液滴入氢氧化钙溶液中,溶液由无色变红色.
(2)除去氢氧化钠溶液中少量的氢氧化钙杂质,实质就是除去钙离子,可利用适量的碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
故答案为:(1)红;(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH.
点评 本题难度不大,掌握碱的化学性质、抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)等是正确解答本题的关键.

练习册系列答案
相关题目
15.对化学的认识不正确的是( )
| A. | 不仅研究自然界已经存在的物质,还要根据需要研究和制造自然界不存在的新物质 | |
| B. | 想制什么物质就可以制什么物质 | |
| C. | 开发新能源和新材料,改善人类的生存条件 | |
| D. | 综合应用自然资源和保护环境,使人类生活得更美好 |
16.已知在反应2A+B=2C中,参加反应的A、B的质量分别是10克和8克,生成的C的质量是( )
| A. | 2×10克+8克=28克 | B. | 10克+8克=18克 | ||
| C. | (2×10克+8克)÷2克=14克 | D. | (10克+8克)÷2=9克 |
20.下列物质中,属于纯净物的是( )
| A. | 自来水 | B. | 酱油 | C. | 米醋 | D. | 冰水混合物 |
10.下列化学方程式符合题意且书写正确的是( )
| A. | 氢气作燃料无污染:2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| B. | 盐酸除铁锈:FeO+2HCl═FeCl2+H2O | |
| C. | 改良酸性土壤的原理:NaOH+HCl═NaCl+H2O | |
| D. | 用磷制作烟幕弹的原理:P+O2$\frac{\underline{\;点燃\;}}{\;}$ P2O5 |
17.住宅和商场等地发生火灾,消防人员用高压水枪喷水灭火,水在灭火中的主要作用是( )
| A. | 降低燃烧物的着火点 | B. | 使大火隔绝空气中的氧气 | ||
| C. | 降低温度到燃烧物着火点以下 | D. | 水分解出不能助燃的物质 |
14.在实验室做化学实验,发生下列事故时,处理方法正确的是( )
| A. | 衣服沾上大量浓氢氧化钠溶液,需将此衣服浸没在盛有水的面盆中 | |
| B. | 皮肤上溅上浓硫酸,用水冲洗 | |
| C. | 不慎将酸液溅到眼中,应立即闭住眼睛,流出眼泪将酸液带出 | |
| D. | 实验桌上酒精灯倾倒,酒精流在桌面上并着火,立即用湿抹布扑灭 |