题目内容
将25克含杂质的大理石放到100克稀盐酸中,恰好完全反应后,产生气体8.8克.求
(1)大理石中碳酸钙的质量分数;
(2)所用稀盐酸的溶质的质量分数.
(1)大理石中碳酸钙的质量分数;
(2)所用稀盐酸的溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:大理石与稀盐酸反应生成氯化钙、水和二氧化碳,由产生二氧化碳气体的质量为8.8g,据此结合反应的化学方程式计算出参加反应的碳酸钙的质量、所用稀盐酸的溶质的质量,进而可计算出溶质的质量分数.
解答:解:设大理石中碳酸钙的质量分数为x,所用稀盐酸的溶质的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 8.8g
=
x=20g
=
y=14.6g
(1)大理石中碳酸钙的质量分数为
×100%=80%.
(2)所用稀盐酸的溶质的质量分数为
×100%=14.6%.
答:(1)大理石中碳酸钙的质量分数为80%;(2)所用稀盐酸的溶质的质量分数为14.6%.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
x y 8.8g
| 100 |
| 44 |
| x |
| 8.8g |
| 73 |
| 44 |
| y |
| 8.8g |
(1)大理石中碳酸钙的质量分数为
| 20g |
| 25g |
(2)所用稀盐酸的溶质的质量分数为
| 14.6g |
| 100g |
答:(1)大理石中碳酸钙的质量分数为80%;(2)所用稀盐酸的溶质的质量分数为14.6%.
点评:本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
X元素的原子结构示意图为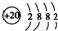 ,元素Y的化合价为-1,由X和Y两种元素形成的化合物的化学式可能是( )
,元素Y的化合价为-1,由X和Y两种元素形成的化合物的化学式可能是( )
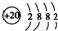 ,元素Y的化合价为-1,由X和Y两种元素形成的化合物的化学式可能是( )
,元素Y的化合价为-1,由X和Y两种元素形成的化合物的化学式可能是( )| A、XY2 |
| B、X2Y |
| C、XY |
| D、XY20 |
下列实验现象描述正确的是( )
| A、红磷燃烧产生大量的白烟 |
| B、硫在空气中燃烧,产生淡蓝色火焰 |
| C、木炭在氧气中燃烧,生成黑色固体 |
| D、电解水时正极产生的气体比负极产生的气体体积多 |
下列符号不具有宏观意义,只有微观意义的是( )
| A、Cu |
| B、O2 |
| C、2H2SO4 |
| D、H2O |
下列推理中正确的是( )
| A、冰和水的混合物中只存在一种分子,所以冰和水的混合物一定属于纯净物 |
| B、单质是由一种元素组成的物质,则由一种元素组成的物质一定是单质 |
| C、因为化学变化中同时发生物理变化,所以化学变化包含物理变化 |
| D、同种元素的原子所含质子数相同,则所含相同质子数的微粒一定属同种元素 |
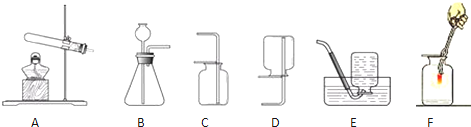
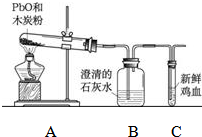 某化学兴趣小组成员小强、小明和小红三位同学在学习了木炭花园氧化铜的实验后,提出如下问题:“木炭与氧化铅(化学式为PbO)反应生成铅的同时,产生的气体一定全部都是二氧化碳吗?”请你和他们一起对产物中气体的成分进行探究,并回答有关问题.
某化学兴趣小组成员小强、小明和小红三位同学在学习了木炭花园氧化铜的实验后,提出如下问题:“木炭与氧化铅(化学式为PbO)反应生成铅的同时,产生的气体一定全部都是二氧化碳吗?”请你和他们一起对产物中气体的成分进行探究,并回答有关问题.