题目内容
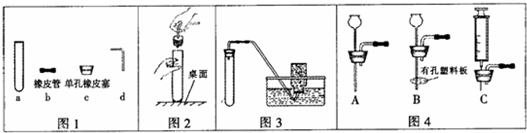
11.如图所示为实验室常见气体制备,净化、干燥、收集和性质实验的部分仪器(组装实验装置时,可重复选择仪器).某学校两个化学实验探究小组的同学欲用他们完成各自的探究实验.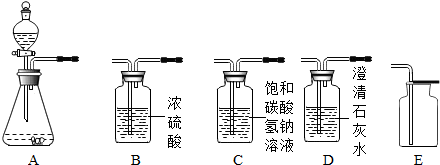
以石灰石和稀盐酸为原料,在实验室中制备、收集干燥纯净的二氧化碳气体,按照要求设计实验装置、连接仪器,并检验装置的气密性.(提示:挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收).
①所选仪器的连接顺序为A→C→B→E(填写仪器序号字母).
②若将二氧化碳通入澄清的石灰水中,石灰水的pH将减小(填“增大”“减小”“不变”之一).
③C中发生反应的化学方程式为NaHCO3+HCl=NaCl+CO2↑+H2O.
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.仪器B中浓硫酸的作用是:吸水或干燥气体;挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收,氯化氢气体溶于水是盐酸,盐酸与碳酸氢钠反应生成氯化钠和水和二氧化碳.
解答 解:①在实验室中制备、收集干燥纯净的二氧化碳气体,装置的连接顺序是:A-C-B-E,要先除杂质再干燥;故答案为:A-C-B-E;
②二氧化碳溶于水生成碳酸,碳酸与氢氧化钙发生综合反应,故石灰水的pH将减小;
③C中挥发出的少量HCl气体可用饱和碳酸氢钠溶液吸收,氯化氢气体溶于水是盐酸,盐酸与碳酸氢钠反应生成氯化钠和水和二氧化碳,反应的方程式为:NaHCO3+HCl=NaCl+CO2↑+H2O.
故答案为:①C、B;②减小;③NaHCO3+HCl=NaCl+CO2↑+H2O.
点评 本题主要考查化学方程式的书写,实验装置的选择,选择发生装置时,要考虑反应物的状态、反应条件等因素;选择收集装置时,要考虑气体的水溶性、能否和水发生化学反应、密度、能否和空气中的物质发生化学反应等因素.

练习册系列答案
相关题目
6.化学肥料对粮食增产起着重要作用,下列物质能用作复合肥的是( )
| A. | KH2PO4 | B. | K2SO4 | C. | NH4HCO3 | D. | Ca3(PO4)3 |
16.下列符号,既能表示一个原子,又能表示一种元素.还能表示一种物质的是( )
| A. | OH- | B. | Cu | C. | O2 | D. | H |
3.如图是两种气体发生化学反应的微观示意图,其中相同的球代表同种原子.下列说法正确的是( )

| A. | 分子在化学变化中不可再分 | |
| B. | 化学反应前后原子的种类和数目都不变 | |
| C. | 该反应是既不是化合反应也不是分解反应 | |
| D. | 反应后生成了两种新的化合物 |
20.水是我们日常生活必不可少的物质,下列有关水的说法正确的是( )
| A. | 活性炭吸附水中的色素和异味是化学变化 | |
| B. | 水通电分解产生氢气和氧气体积比为2:1 | |
| C. | 水是由氢原子和氧原子组成的 | |
| D. | 用过滤的方法可以使硬水软化 |
1.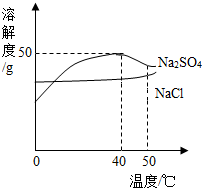 如图是硫酸钠和氯化钠的溶解度曲线,下列说法正确的是( )
如图是硫酸钠和氯化钠的溶解度曲线,下列说法正确的是( )
 如图是硫酸钠和氯化钠的溶解度曲线,下列说法正确的是( )
如图是硫酸钠和氯化钠的溶解度曲线,下列说法正确的是( )| A. | 温度升高两种物质的溶解度都增大 | |
| B. | 50℃的Na2SO4饱和溶液降到40℃时有晶体析出 | |
| C. | 40℃时,Na2SO4的饱和溶液中溶质与溶剂的质量比为1:2 | |
| D. | 可用降温结晶的方法提纯含少量Na2SO4的NaCl |