题目内容
6.钠(Na)是一种非常活泼的金属.钠在空气中极易氧化,迅速失去金属光泽,所以钠不能露置于空气中,而应贮存在煤油里.【演示实验】在烧杯中加一些水,滴入几滴酚酞溶液,然后把一小块钠放入水中.
【实验现象】钠浮在水面上,熔成小球,四处游动,发出哧哧响声,越来越小直至消失,溶液颜色变红.
【实验结论】钠能与水发生剧烈的化学反应生成氢氧化钠(NaOH)和氢气.
(1)试写出钠与水反应的化学方程式.
(2)将4.6克钠放入95.4克水中,完全反应后所得溶液中溶质的质量分数是多少?
分析 (1)写出化学方程式.
(2)写出化学方程式并代入钠的质量计算出氢氧化钠的质量、氢气的质量,然后计算出反应后溶液的质量.
解答 解:(1)钠能与水发生剧烈的化学反应生成氢氧化钠(NaOH)和氢气,反应的化学方程式为:2Na+2H2O═2NaOH+H2↑
(2)设氢氧化钠的质量为x,氢气的质量为y.
2Na+2H2O═2NaOH+H2↑
46 80 2
4.6g x y
$\frac{46}{4.6g}=\frac{80}{x}=\frac{2}{y}$
x=8.0g
y=0.2g
(2)反应后溶液的质量=95.6g+4.6g-0.2g=100g,则溶液中氢氧化钠的质量分数=$\frac{8g}{100g}$×100%=8%.
答案:
(1)2Na+2H2O═2NaOH+H2↑;
(2)完全反应后所得溶液中溶质的质量分数是8%.
点评 本题较简单,可直接利用化学方程式来计算,但应注意计算格式要规范,向规范要质量.掌握化学方程式的计算格式和规范性,本题的关键是计算出反应后溶液的质量.

练习册系列答案
相关题目
17.对天宫一号目标飞行器内镍氢电池的总反应式:H2+2NiO(OH)=2Ni(OH)2,下列叙述不正确的是( )
| A. | H2是非金属单质 | |
| B. | H元素与Ni 元素在反应前后化合价均发生变化 | |
| C. | NiO(OH)中Ni化合价为+2价 | |
| D. | 该反应为化合反应 |
11.学好化学,就要学会归纳和总结,下列总结有错误的一组是( )
| A | 安全常识 | B | 生活知识 |
| 瓦斯爆炸──天然气引起 煤气中毒──CO引起 | 硬水──可溶性的钙镁化合物含量高 蜂窝煤易于燃烧──与空气充分接触 | ||
| C | 物质的性质与用途 | D | 物质分类 |
| H2作高能燃料──可燃性 N2作保护气──化学性质不活泼 | 空气──混合物 河水──氧化物 |
| A. | A | B. | B | C. | C | D. | D |
18.下列图象不能正确反映对应变化关系的是( )
| A. |  向一定量的二氧化锰中加入过氧化氢溶液 向一定量的二氧化锰中加入过氧化氢溶液 | |
| B. |  向稀盐酸中滴加氢氧化钠溶液 向稀盐酸中滴加氢氧化钠溶液 | |
| C. |  向两份完全相同的稀硫酸中分别加入足量镁粉、铁粉 向两份完全相同的稀硫酸中分别加入足量镁粉、铁粉 | |
| D. |  将水通电一段时间 将水通电一段时间 |
15.逻辑推理是一种重要的化学思维方法.以下推理合理的是( )
| A. | 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有C和H | |
| B. | 因为中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 | |
| C. | 因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 | |
| D. | 因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液 |
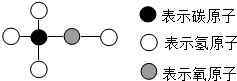 长江商报消息3月23日起,宜昌市五峰土家族自治县相继发生散装白酒致人死亡事件,至25日晚10时,已有4人因疑似甲醇中毒死亡,甲醇有剧毒,不能食用,其分子结构可如图所示的模型表示.从模型可看出甲醇由三种元素组成,其的化学式为CH4O.
长江商报消息3月23日起,宜昌市五峰土家族自治县相继发生散装白酒致人死亡事件,至25日晚10时,已有4人因疑似甲醇中毒死亡,甲醇有剧毒,不能食用,其分子结构可如图所示的模型表示.从模型可看出甲醇由三种元素组成,其的化学式为CH4O.