题目内容
16.某化学探究小组为了验证铁、铜、锌、银的金属活动性顺序,设计了如下实验方案:
①将铁片加入到稀盐酸中;②将铜片加入到硝酸银溶液中;③将锌片加入到稀盐酸中;④将金属片X加入到Y中.(所有金属均已打磨,且形状、大小以及稀盐酸浓度均相同)
(1)写出①中反应的化学方程式:Fe+2HCl═FeCl2+H2↑;
(2)通过上述实验,可以判断锌的金属活动性比铁强,依据的现象是锌与稀盐酸反应产生气泡的速率较快,而铁与稀盐酸反应产生气泡的速率较慢;
(3)要得出这四种金属的活动性顺序,如果④中Y表示硫酸铜溶液,则X表示的一种金属是铁.
分析 我们在判断金属活动性的强弱的时候,所进行的操作通常有两种方法:一是让金属与酸反应,然后根据反应的速率即产生气泡的快慢来进行判断,反应越剧烈活泼性越强,二是把一种金属放入另一种金属的盐的溶液中,看是否能够置换出溶液中的金属,来判断它们的活动性,本题可以根据这两个要素来答题.
解答 解:(1)将铁片加入稀盐酸中,铁要与稀盐酸反应生成氢气,所以,①中反应的化学方程式为:Fe+2HCl═FeCl2 +H2↑;
(2)由于金属铁和锌都能够和稀盐酸反应,那么我们判断它们强弱的先后顺序的依据就是:它们与盐酸反应时产生氢气速率的快慢,产生氢气的速率越快,则活动性越强.所以,可以判断锌的金属活动性比铁强,依据的现象是:锌与稀盐酸反应产生气泡的速率较快,而铁与稀盐酸反应产生气泡的速率较慢
(3)在这里我们根据所给的三个实验,我们可以判断出锌比铁活泼,铜比银活泼,在这里我们只要验证一下铁和铜谁更活泼即可,方法同样是两种:一是可以让铜和稀盐酸反应,二是让铜与铁的盐溶液,或是让铁与铜的盐溶液进行反应,看能否置换出相应的金属单质,所以,如果④中Y表示硫酸铜溶液,则X表示的一种金属是铁.
故答为:(1)Fe+2HCl═FeCl2+H2↑;(2)锌与稀盐酸反应产生气泡的速率较快,而铁与稀盐酸反应产生气泡的速率较慢;(3)铁;
点评 本题考查学生对于金属活动性顺序的探究,我们可以把这类题目归结为“明知故问”型的题目,我们在解答该类题目时就是根据已经掌握的金属活动性顺序,然后选择合适的酸或者是盐的溶液来进行解答.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.据图可得出的结论中正确的是( )
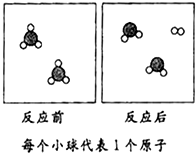

| A. | 该反应是化合反应 | |
| B. | 该反应的反应物一定是氧化物 | |
| C. | 该反应是分解反应 | |
| D. | 该反应中反应物和生成物的分子个数比为1:1:1 |
8.下列有关的说法正确的是( )
| A. | 废旧电池可随意丢弃,不会对环境造成污染 | |
| B. | 生铁和钢都是铁的合金 | |
| C. | 多数合金的熔点高于它的成分金属 | |
| D. | 地壳中含量最多的金属元素是铁元素 |
6.善于用化学的眼光看世界,能够提高我们的科学素养.你认为下列变化事实和相应解释不一致的是( )
| 事实 | 解释 | |
| A | 50mL水和50mL酒精混合后体积小于100mL | 分子之间有间隔 |
| B | 敞口放置的浓盐酸逐渐变稀 | 分子是不断地运动的 |
| C | 液态水和固态冰状态有差异 | 构成它们的分子不同 |
| D | 温度计中的水银(汞)热胀冷缩 | 原子之间的间隔发生了变化 |
| A. | A | B. | B | C. | C | D. | D |


 有A、B、C、D、E五种物质,在常温下A、B是液体,C是气体,D是黑色固体,E是一种能使澄清石灰水变浑浊的气体;A和B的组成元素相同,图中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.
有A、B、C、D、E五种物质,在常温下A、B是液体,C是气体,D是黑色固体,E是一种能使澄清石灰水变浑浊的气体;A和B的组成元素相同,图中“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.