题目内容
某同学用纯碱溶液和澄清的石灰水制取烧碱,充分搅拌后过滤,对滤液的组成作了如下猜想:
(1)【猜想一】溶质为氢氧化钠;【猜想二】溶质为氢氧化钠和氢氧化钙
【猜想三】溶质为 .
(2)如果猜想三成立,请根据下表要求,设计实验方案进行验证.
(3)该同学作出猜想一的理由是: .
(4)请写出该同学制取烧碱的反应方程式: .
(1)【猜想一】溶质为氢氧化钠;【猜想二】溶质为氢氧化钠和氢氧化钙
【猜想三】溶质为
(2)如果猜想三成立,请根据下表要求,设计实验方案进行验证.
| 实验操作方法 | 实验现象 | 实验结论 |
| 取少量滤液,滴加足量的 | 猜想三成立 |
(4)请写出该同学制取烧碱的反应方程式:
考点:实验探究物质的组成成分以及含量,碱的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:碳酸钠溶液与澄清石灰水反应会出现三种情况:其一,两溶液恰好完全反应,反应后的溶液中只含有氢氧化钠;其二,澄清石灰水过量,反应后的溶液中除生成的氢氧化钠外还含有未反应的氢氧化钙;其三,碳酸钠溶液过量,反应后的溶液中除生成的氢氧化钠外还含有未反应的碳酸钠.可采取向滤液样品中滴加稀盐酸或澄清石灰水的方法,检验反应后溶液中是否含有碳酸钠,根据反应写出反应的化学方程式.
解答:解:(1)碳酸钠溶液与澄清石灰水可能恰好完全反应,形成氢氧化钠溶液;或者澄清石灰水过量,形成氢氧化钠与氢氧化钙的混合溶液;或者碳酸钠溶液过量,形成氢氧化钠与碳酸钠的混合溶液.所以,【猜想三】溶质为:氢氧化钠和碳酸钠.
(2)由于碳酸钠溶液能与稀盐酸(或氢氧化钙)反应生成了气泡(沉淀),所以,实验方案为:
(3)由上述分析可知,该同学作出猜想一的理由是:当纯碱溶液和澄清的石灰水两溶液恰好完全反应时,反应后的溶液中只含有氢氧化钠.
(4)该同学制取烧碱的反应方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
故答为:(1)氢氧化钠和碳酸钠;(2)见上表;(3)当纯碱溶液和澄清的石灰水两溶液恰好完全反应时,反应后的溶液中只含有氢氧化钠.(4)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)由于碳酸钠溶液能与稀盐酸(或氢氧化钙)反应生成了气泡(沉淀),所以,实验方案为:
| 实验操作方法 | 实验现象 | 实验结论 |
| 取少量滤液,滴加足量的 稀盐酸溶液; | 有气泡产生 | 猜想三成立 |
(4)该同学制取烧碱的反应方程式:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
故答为:(1)氢氧化钠和碳酸钠;(2)见上表;(3)当纯碱溶液和澄清的石灰水两溶液恰好完全反应时,反应后的溶液中只含有氢氧化钠.(4)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
点评:根据反应物的过量情况,反应会出现多种结果,据此对反应后的生成物的可能组成进行猜想.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
欲除去括号内的少量杂质,选用的试剂不正确的是( )
| A、NaOH溶液(Na2CO3)加入适量稀盐酸 |
| B、O2(H2O)通过浓硫酸 |
| C、CO(CO2)通过浓碱溶液 |
| D、Cu(Fe)加入适量稀盐酸 |
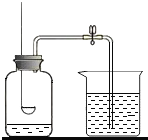 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格,并与同学交流.