题目内容
12.实验开放日,小佳取50g硫酸溶液与50g氯化钡溶液混合,恰好完全反应,反应后得到溶液95.34g,求小佳所用硫酸的溶质质量分数.分析 由于硫酸与氯化钡反应生成了硫酸钡沉淀,混合液减少的质量就是生成的沉淀硫酸钡的质量,根据硫酸钡的质量可求出硫酸溶液中溶质的质量,再根据溶质的质量分数求出所用硫酸的溶质质量分数.
解答 解:由题意可知,生成的沉淀的质量为:50g+50g-95.34g=4.66g
设硫酸溶液中溶质的质量为x:
H2SO4+BaCl2═BaSO4↓+2HCl
98 233
x 4.66g
$\frac{98}{233}=\frac{x}{4.66g}$ 解得:x=0.98g
硫酸溶液中H2SO4的质量分数为:$\frac{0.98g}{50g}$×100%=1.96%
答:小佳所用硫酸的溶质质量分数是1.96%.
点评 根据化学方程式进行计算的步骤一般为设出未知数,写出配平的化学方程式,求出相关物质的质量比,列出比例式,求解,答,共六步.

练习册系列答案
相关题目
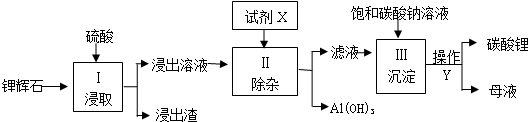
2.碳酸锂广泛应用于陶瓷和医药等领域.以锂辉石(主要成分为Li2O-Al2O3-4SiO2)为原材料制备Li2CO3的部分工艺流程如下:
已知:①某些物质的溶解度(S)如表
②Li2O•Al2O3•4SiO2+4H2SO4═Li2SO4+Al2(SO4)3+4SiO2↓+4H2O
请回答:
(1)步骤Ⅰ中锂辉石要粉碎成细颗粒的目的是增大接触面积,使反应充分进行,加入稍过量的硫酸后所得浸出液的溶质有H2SO4、Li2SO4、Al2(SO4)3.
(2)步骤Ⅱ中,加入的试剂X应显碱性.(填“酸”或“碱”)
(3)步骤Ⅲ中,生成沉淀的化学方程式为Na2CO3+Li2SO4═Li2CO3↓+Na2SO4.
(4)在实验室,操作Y的名称是过滤.
(5)操作Y后所得固体需要洗涤,下列洗涤剂合适的是A.
A.热蒸馏水 B.稀硫酸 C.冷蒸馏水 D.饱和碳酸钠溶液
为检验固体是否洗涤干净,可取最后一次洗涤液,加入BaCl2,观察是否有沉淀产生.

已知:①某些物质的溶解度(S)如表
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
请回答:
(1)步骤Ⅰ中锂辉石要粉碎成细颗粒的目的是增大接触面积,使反应充分进行,加入稍过量的硫酸后所得浸出液的溶质有H2SO4、Li2SO4、Al2(SO4)3.
(2)步骤Ⅱ中,加入的试剂X应显碱性.(填“酸”或“碱”)
(3)步骤Ⅲ中,生成沉淀的化学方程式为Na2CO3+Li2SO4═Li2CO3↓+Na2SO4.
(4)在实验室,操作Y的名称是过滤.
(5)操作Y后所得固体需要洗涤,下列洗涤剂合适的是A.
A.热蒸馏水 B.稀硫酸 C.冷蒸馏水 D.饱和碳酸钠溶液
为检验固体是否洗涤干净,可取最后一次洗涤液,加入BaCl2,观察是否有沉淀产生.
7.某同学在厨房进行的活动,其中不涉及化学变化的是( )
| A. | 用食醋除去暖水瓶中的水垢 | B. | 将土豆切成丝状 | ||
| C. | 切过水果的菜刀未处理而生锈 | D. | 和面时加入纯碱除去馒头的酸味 |
17.分析推理是化学学习和研究中常用的思维方法.下列分析推理正确的是( )
| A. | 因为甲醛能使蛋白质变性,起到防腐作用,所以甲醛水溶液可用于浸泡水产品 | |
| B. | 降低温度能够灭火,所以油锅着火可以用浇水降温的方法灭火 | |
| C. | 酸能够使紫色石蕊溶液变红,二氧化碳能使紫色石蕊溶液变红色,所以二氧化碳是酸 | |
| D. | 氧化物中含有氧元素,但是含有氧元素的化合物不一定是氧化物 |
4.洗涤与生活密切相关.下列洗涤方法中利用乳化原理的是( )
| A. | 用汽油洗涤油污 | B. | 用洗洁精清洗餐具 | ||
| C. | 用盐酸清洗水垢 | D. | 用酒精洗去试管中的碘 |