题目内容
14.将一定量的金属M(M是Mg、Al、Zn、Fe中的一种)粉末放入AgNO3和Cu(NO3)2的混合溶液中,充分反应后过滤,得到滤渣和无色滤液.向滤渣和滤液中分别滴加稀盐酸均无明显现象产生.(1)金属M不可能是铁(填名称).
(2)滤渣中一定含有的金属是银、铜;无色滤液中含有的阴离子是NO3-(填符号)
分析 镁比铝活泼,铝比锌活泼,锌比铁活泼,都能够和硝酸银、硝酸铜反应;
硝酸铜溶液是蓝色溶液,硝酸亚铁溶液是浅绿色溶液;
Mg、Al、Zn、Fe都能够和稀盐酸反应生成盐和氢气,而Ag和Cu都不能和稀盐酸反应.
解答 解:(1)充分反应后过滤,得到无色滤液,说明硝酸铜已经完全反应,金属M不可能是铁,这是因为铁能和硝酸银、硝酸铜反应生成硝酸亚铁,而硝酸亚铁溶液是浅绿色溶液.
故填:铁.
(2)充分反应后过滤,得到无色滤液,说明硝酸铜已经完全反应,而硝酸银先于硝酸铜反应,因此硝酸银也已经完全反应,滤渣中一定含有的金属是反应生成的银和铜,向滤渣和滴加稀盐酸无明显现象产生,说明滤渣中不含有Mg、Al、Zn、Fe;
无色滤液中含有的阴离子是硝酸根离子,可以表示为.
故填:银、铜;NO3-.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
5.现有60℃的饱和硝酸钾溶液,欲降低其溶质质量分数,下列方法可行的是( )
| A. | 加入一定量的硝酸钾 | B. | 恒温蒸发部分水 | ||
| C. | 升温到80℃ | D. | 加入一定量的氯化钠 |
9.生活离不化学,化学与生活息息相关.
(1)人体可以从水果和蔬菜中摄取维生素,该类物质需要量很小,但可以起到调节新陈代谢、预防疾病和维持身体健康的作用.
(2)如表是某儿童补铁药品的部分说明.说明中的“铁”指的是元素(填“单质”、“元素”或“分子”).
(3)某些食品的近似pH如下:
其中酸性最强的是柠檬汁,胃酸过多的人应食用玉米粥.
(4)农业上用石灰乳和硫酸铜配制农药“波尔多液”时不宜用铁质容器,用化学方程式表示其原因Fe+CuSO4=Cu+FeSO4.
(5)如图为某化工企业生产流程示意图:下列说法正确的是D.(填选项序号)
A.钛酸亚铁(FeTiO3)中钛元素为+3价
B.③中氩气(Ar)作反应物,反应类型为置换反应
C.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
D.①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X为FeCl3.
(1)人体可以从水果和蔬菜中摄取维生素,该类物质需要量很小,但可以起到调节新陈代谢、预防疾病和维持身体健康的作用.
| 营养成分表 | ||
| 营养成分 | 每片含量 | 每100g含量 |
| 镁 | 6.7mg | 1.12g |
| 叶酸 | 255 | 42.5mg |
(3)某些食品的近似pH如下:
| 食品 | 柠檬汁 | 苹果汁 | 葡萄汁 | 番茄汁 | 牛奶 | 玉米粥 |
| pH | 2.4 | 3.1 | 4.2 | 4.4 | 6.5 | 7.8 |
(4)农业上用石灰乳和硫酸铜配制农药“波尔多液”时不宜用铁质容器,用化学方程式表示其原因Fe+CuSO4=Cu+FeSO4.
(5)如图为某化工企业生产流程示意图:下列说法正确的是D.(填选项序号)

A.钛酸亚铁(FeTiO3)中钛元素为+3价
B.③中氩气(Ar)作反应物,反应类型为置换反应
C.②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2
D.①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X为FeCl3.
6.下列化学用语书写正确的是( )
| A. | 3个硫酸根离子:3SO4-2 | |
| B. | 2个镁原子:Mg2 | |
| C. | 五氧化二磷分子:O2P5 | |
| D. | 标出氯化钙中氯元素的化合价:Ca$\stackrel{-1}{C{l}_{2}}$ |
3.将一定量的锌粉加入到Mg(NO3)2、Cu(NO3)2、AgNO3三种物质的混合溶液中充分反应后过滤,将滤渣放入稀盐酸溶液里,有气泡产生.则下列情况不可能存在的是( )
| A. | 滤渣是Ag、Cu、Zn | B. | 滤渣是Ag、Cu、Mg | ||
| C. | 滤液中含有Zn2+、Mg2+、NO3- | D. | 金属活动性顺序是Ag<Cu<Zn<Mg |
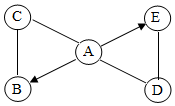 A、B、C、D、E为初中化学常见的五种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连物质能发生化学反应,部分反应物、生成物及反应条件已略去).
A、B、C、D、E为初中化学常见的五种物质,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“-”表示相连物质能发生化学反应,部分反应物、生成物及反应条件已略去).